表1 Plackett-Burman 试验因素与水平设置
Table 1 Factors and levels of Plackett-Burman experiment

编号因素低水平(−1)高水平(+1) A褐藻胶(g/L)1015 B硫酸铵(g/L)7.59.0 C氯化钠(g/L)1520 D磷酸二氢钾(g/L)57.5 E虚拟1−1+1 F硫酸镁(g/L)0.40.5 GpH7.58.5 H温度(°C)2530 I接种量(%)1.52.0 K虚拟2−1+1
北京大学学报(自然科学版) 第61卷 第6期 2025年11月
Acta Scientiarum Naturalium Universitatis Pekinensis, Vol. 61, No. 6 (Nov. 2025)
doi: 10.13209/j.0479-8023.2025.101
摘要 以褐藻胶作为选择性培养基的唯一碳源, 从海藻中分离筛选出一株具有良好褐藻胶降解能力的微生物菌株。通过生理生化鉴定、16S rDNA 序列分析以及全基因组测序, 对该菌株进行系统的鉴定和生物信息学分析, 揭示可能的褐藻胶裂解酶相关基因。此外, 通过单因素试验、Plackett-Burman 设计和响应面法对该菌株的产酶条件进行优化。形态学观察、生理生化特征分析及 16S rDNA 基因序列鉴定结果确认该菌株为科贝特氏菌属。该菌株基因组全长为 4136490bp, GC 含量为 62.48%。基因组预测编码 3454 个蛋白编码基因, 70 个tRNA 基因和 12 个 rRNA 基因。随后进行核苷酸一致性分析, 将其命名为 Cobetia marina 29。在基因功能注释方面, 通过 GO, KEGG, COG 和 CAZy 数据库, 分别识别出 2487, 2271, 2910 和 145 个具有特定功能的基因, 其中 3 个基因编码褐藻胶裂解酶, 分别属于 PL17 和 PL7 家族。最后, 对培养条件进行优化, 在最佳产酶条件下, 酶活性提高至 179.29U/mL, 比优化前提高 53.6%。研究结果为褐藻胶的生物降解提供了新的菌种资源, 并为后续工业化应用奠定基础。
关键词 褐藻胶裂解酶; 菌株筛选; 全基因组测序; 产酶优化
海藻酸钠, 亦称褐藻胶, 是褐藻中含量最高的多糖(约占干重的 40%)。其结构由 β-D-甘露糖醛酸(M)和 α-L-古罗糖醛酸(G)单体单元组成, 形成聚 α-L-古罗糖醛酸(polyG)、聚 β-D-甘露糖醛酸(polyM)和异聚 MG(polyMG)3 种嵌段结构[1–2]。褐藻胶主要从褐藻中提取, 也可由假单胞菌属(Pseudomonas)和固氮菌属(Azotobacter)等细菌产生[3]。因其特殊的物理性质, 褐藻胶在食品、印刷和制药工业中广泛用作稳定剂、乳化剂和凝胶形成剂[4–5]。此外, 其优良的黏附性、易混合性、低成本及保质期长等特点, 使其成为制备口腔、鼻、眼和胃肠道药物剂型的理想原料[6]。然而, 其高分子量、低吸收率以及提取过程对分子结构和功能性质产生的显著不利影响[7], 限制了其进一步应用。为克服这些局限, 研究者们将目光投向褐藻寡糖(alginate oligosaccha-rides, AOS)的制备, 通过将高分子褐藻胶降解为低分子寡糖, 提高其生物安全性、生物相容性和生物利用度[8]。褐藻寡糖的制备方法主要包括糖苷键水解和生物有机合成[9–10]。糖苷键水解是通过物理方法、化学方法或酶解法来断裂褐藻胶分子中的糖苷键, 生物有机合成则是利用微生物或酶催化合成寡糖。相对于物理方法和化学方法, 酶解法具有能耗低、经济环保、产物纯度高、更适用于工业生产和能够针对性地合成目标寡糖等特性, 因此具有极大的研究意义和应用潜力[11–13]。
褐藻胶裂解酶是一种通过 β-消除反应降解褐藻胶来生成不饱和寡糖的多糖裂解酶[14]。因底物的特异性, 不同来源的褐藻胶裂解酶对特定结构的褐藻胶(如聚甘露糖醛酸和聚古罗糖醛酸)表现出不同的催化效率[15]。部分酶在高温或极端条件下仍然能够保持较高的活性, 显示出良好的工业应用潜力[16–17]。目前已鉴定出超过 1774 个褐藻胶裂解酶序列, 分布在 7 个 PL 家族中[18–19], 主要来源于细菌, 如弧菌属(Vibrio sp. O2)[20]、固氮菌属(Azoto-bacter vinelandii)[21]、假单胞菌属(Pseudomonas sp. Os-ALG-9)[22]以及链霉菌属(Streptomyces sp. ALG-5)[23]等。然而, 现有褐藻胶裂解酶普遍存在酶催化效率较低、底物结构选择性较高和发酵成本高等问题, 工业化应用受到限制。因此, 筛选新的高效降解褐藻胶菌株并优化其产酶条件, 是实现工业化生产的关键。
本研究中, 我们从海藻中筛选出一株高效降解褐藻胶的微生物菌株 Cobetiamarina 29, 通过单因素和响应面优化实验确定其最优产酶条件。Cobe-tiamarina 29 可为褐藻胶的生物降解提供高效酶源, 并为后续构建工程菌奠定基础。
海藻酸钠购自上海阿拉丁试剂有限公司, 磷酸二氢钾、氢氧化钠、酒石酸钾钠、硫酸铵、硫酸镁、硫酸亚铁、氯化钠、氢氧化钠和丙三醇(甘油)购自天津市科密欧化学试剂有限公司, 琼脂购自福州省泉州市泉华港工厂。琼脂为生物试剂, 其余均为分析纯。
液体(富集、复筛)培养基: 褐藻胶 15g/L, 硫酸铵 7.5g/L, 氯化钠 15g/L。固体(初筛)培养基: 褐藻胶 15g/L, 硫酸铵 7.5g/L, 氯化钠 15g/L, 琼脂 20g/L。培养基 pH 均为 7.5。
所用仪器包括 H1750R 台式高速冷冻离心机(湖南湘仪实验室仪器开发有限公司)、F50TECAN酶标仪(瑞士帝肯有限公司)、梯度 PCR 仪(Eppen-dorf 生命科学公司)和 PHS-3C 型精密 pH 计(上海精密科学仪器有限公司)。
在大连近海多个海域采集海水与腐烂的海带样品。取每个海水样品 1mL 和腐烂海带 0.5g, 置于装有富集培养基的锥形瓶中, 并设置对照组(不添加海带样品), 30℃和 200r/min 条件下振荡培养。
初筛: 将浑浊的富集培养液用无菌水稀释至原始浓度的 10−1~10−4倍, 在初筛平板上涂布 100μL 稀释液, 于 30°C 培养 48 小时; 用 95%乙醇处理平板, 观察并记录菌落水解圈直径[24]。
复筛: 选取初筛平板上具有较大水解圈的菌落, 接种至液体培养基中, 在 30°C 和 200r/min 条件下培养至发酵液出现浑浊, 取 1mL 发酵液, 离心后测定上清液中褐藻胶裂解酶的活力, 作为菌株的复筛 指标。
对接种于固体培养基上的菌株进行清洗后, 用2.5%戊二醛固定, 通过乙醇浓度递增的脱水步骤和干燥过程处理后, 在扫描电子显微镜下对样本进行形态观察[25]。使用《常见细菌系统鉴定手册》[26]的方法, 鉴定菌株的生理生化特性。
用 16S rDNA 基因测序法进行菌种鉴定。将菌株在 30°C 和 200r/min 条件下发酵培养 24 小时, 用细菌基因组提取试剂盒提取菌株基因组[27]。采用16S rDNA 基因通用引物[28]进行扩增。PCR 反应体系(25μL): ddH2O 16.75μL, 10×Buffer 2.5μL, DNA 模版 2.5μL, dNTP 2mL, P1 0.5μL, VrTaq E 0.25μL。PCR 扩增条件: 94°C DNA 变性 6min; 53°C 退火 1min, 72°C 延伸 1min, 进行 30 个循环; 72°C 再延伸10min; 4°C 保存。
使用 2%的琼脂糖凝胶电泳检测 PCR 扩增产物, 并将产物送至上海生工生物工程股份有限公司进行测序, 将测得的数据上传至 NCBI 网站, 通过BLAST 软件进行 16S rDNA 序列比对, 并用 MEGA软件绘制系统发育树。
菌液样本送至北京诺禾致源科技股份有限公司, 采用二代测序方法(Illumina 平台)进行测序, 得到 clean date。用 SOAP denovo, SPAdes 和 ABySS 软件进行基因组组装, 并通过 CISA 软件整合结果, 选择包含 scaffold 数量最少的组装结果, 然后使用gapclose 软件(Version:1.12)对组装结果进行缺口填补[29–31], 获得最终的基因组组装结果。
分别采用 GeneMarkS (http://topaz.gatech.edu/)、RepeatMasker 软件, 识别并注释编码基因中重复序列; 利用 tRNAscan-SE 和 rRNAmmer 软件识别并预测非编码 RNA 基因, 包括 tRNA 和 rRNA[32–33]; sRNA 先在 Rfam 数据库比对注释, 接着用 cmsearch程序确定最终的 sRNA。此外, 分别用 IslandPath-DIOMB 软件和 phiSpy 工具对基因岛和前噬菌体进行预测[34]。
参照潘琳[35]的方法, 对预测到的编码基因蛋白序列在不同数据库中的蛋白质序列进行 BLAST 比对。
参照成珍[36]测酶活性的方法, 取 1mL 发酵上清液。将 20μL 上清液与 180μL 底物 40°C 反应 30min(对照组取灭活后的上清液)。反应结束后, 与200μL 3,5-二硝基水杨酸(DNS)反应, 测定 540nm处的吸光度。
将每分钟催化产生 1µg 还原糖所需的酶量定义为一个酶活力单位(U), 计算公式为
酶活力(U/mL)=1000mN/(tV) , (1)
式中, N为稀释倍数, m为还原糖量(mg), t为反应时间(min), V为酶液体积(mL)。
1)单因素试验。初始培养条件设为 30°C, 200r/min 培养 24 小时。在培养基中分别以 15.0g/L 的褐藻胶、蔗糖、淀粉、麦芽糖和葡萄糖为唯一碳源, 用来确定该菌种的最佳碳源。再分别以 7.5g/L的硫酸铵、氯化铵、蛋白胨、牛肉膏和酵母浸粉为唯一氮源, 用来确定其最适氮源。在此基础上, 考虑以下 8 个因素对酶活性的影响: 褐藻胶(5.0~40.0g/L)、硫酸铵(2.5~12.5g/L)、氯化钠(5.0~25.0g/L)、磷酸二氢钾(0~10.0g/L)、硫酸镁(0~1.0g/L)、pH (5.5~9.5)、温度(10~50°C)和接种量(0.5%~2.5%)。
2)Plackett-Burman 试验。采用 Minitab 软件设计 Plackett-Burman 试验, 探究单因素实验确定的 8个因素对酶活的影响。取每个因素的两个水平, 二者相差 1.0~1.5 倍, 设置 3 组平行试验。同时设两个虚拟因素来比较实验中的误差。以褐藻胶裂解酶的活性为响应指标, 设计方案见表1。
3)响应面试验。利用 Design-Expert 软件设计响应面优化试验(表2), 以褐藻胶裂解酶活性(Y)为响应值, 以硫酸铵(A)、pH(B)和温度(C)为主要因素, 设计三因素三水平的试验, 优化褐藻胶降解菌Cobetia marina 29 的产酶条件, 设 3 组平行实验。
表1 Plackett-Burman 试验因素与水平设置
Table 1 Factors and levels of Plackett-Burman experiment

编号因素低水平(−1)高水平(+1) A褐藻胶(g/L)1015 B硫酸铵(g/L)7.59.0 C氯化钠(g/L)1520 D磷酸二氢钾(g/L)57.5 E虚拟1−1+1 F硫酸镁(g/L)0.40.5 GpH7.58.5 H温度(°C)2530 I接种量(%)1.52.0 K虚拟2−1+1
表2 响应面试验因素与水平设置
Table 2 Factors and levels of response surface experiment
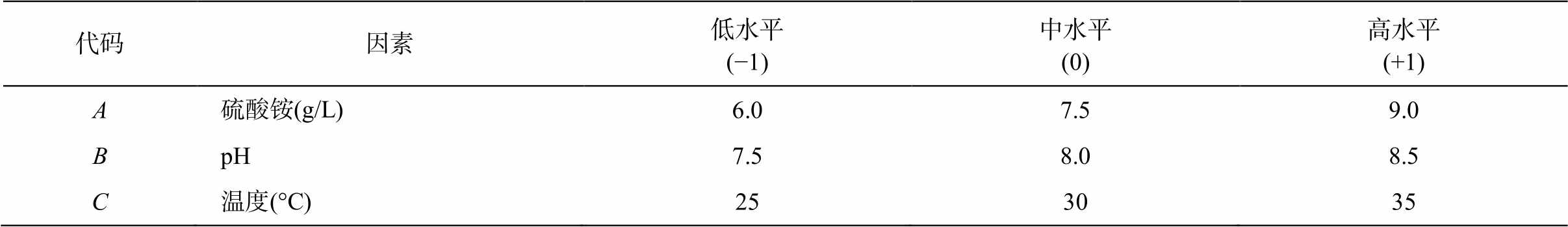
代码因素低水平(−1)中水平(0)高水平(+1) A硫酸铵(g/L)6.07.59.0 BpH7.58.08.5 C温度(°C)253035
采用 Minitab 和 Design-Expert 两种软件进行数据的处理和分析。
通过富集培养与初筛, 获得具有明显透明圈的褐藻胶降解菌株[37], 从中选取 74 个菌落(17 个霉菌和 57 个细菌)进行复筛。本研究以发酵液稀释程度、菌液浑浊度以及菌体附着情况为指标(以未接菌的发酵液作为对照), 评估降解菌的产酶活性。实验结果显示, 细菌发酵液在 12 小时后显著稀释, 菌液浑浊且菌体附着明显, 霉菌发酵液则在 48 小时后才呈现类似的变化。据此推测, 霉菌产酶活性可能低于细菌在褐藻胶降解方面的表现。随后, 对所筛选的菌株进行酶活性测定, 并汇总酶活力较高的菌株。如表3 所示, 编号为 29 的菌株展现出最高的酶活性, 其值达到 116.73U/mL。因此, 选择 29 号菌株进行后续研究。
2.1.1 生理生化及形态学鉴定
在固体培养基上培养两天后, 29 号菌株的菌落特征如图 1(a)所示。菌落呈现规则的乳白色圆形轮廓, 并在其周围形成清晰可见的环状透明圈。菌落表面光滑, 各个菌落之间界限清晰。扫描电子显微镜分析结果如图 1(b)所示, 菌体长度约 1.5μm, 呈不规则直杆状。
表3 单菌落酶活力
Table 3 Enzyme activity of bacterial colonies
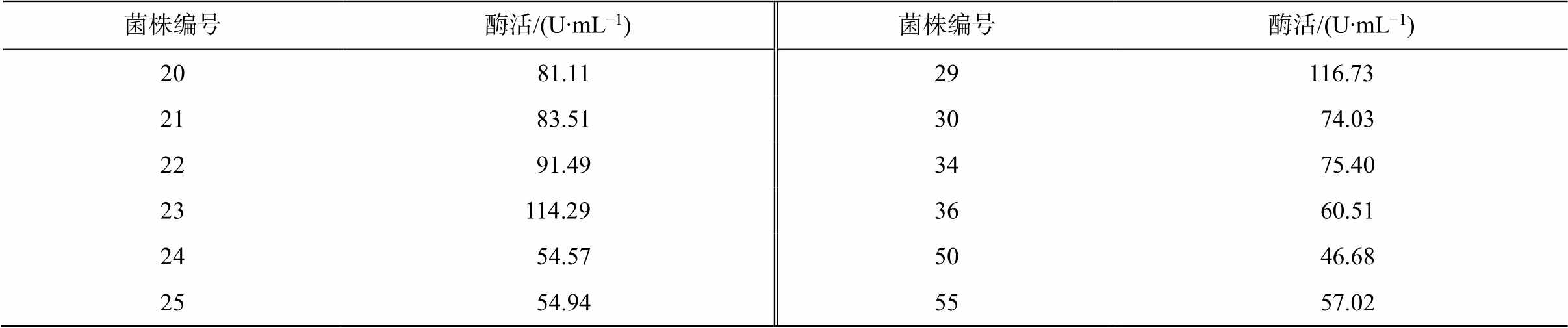
菌株编号酶活/(U∙mL−1)菌株编号酶活/(U∙mL−1) 20 81.1129116.73 21 83.5130 74.03 22 91.4934 75.40 23114.2936 60.51 24 54.5750 46.68 25 54.9455 57.02
该菌株的生理生化特征见表4。菌株 29 显示出盐耐受性, 能够以葡萄糖、蔗糖为碳源进行生长, 但不能将乳糖、木糖和可溶性淀粉作为碳源, 这一生理生化特性与 Arahal 等[38]描述的海科贝特氏菌模式菌株 Cobetia marina DSM 4741T相符。然而, 在明胶液化实验中存在差异, 菌株 29 表现出阳性反应, 表明其具备降解明胶的能力。
2.1.2 16S rDNA鉴定结果
将菌株 29 进行 DNA 提取后, 通过 PCR 扩增并测序, 采用分子生物学方法鉴定其 16S rDNA 基因序列, 长度为 1500bp。在 NCBI 数据库中进行序列比对分析, 结果显示菌株 29 的 16S rDNA 与 Cobetia marina strain KMM3879的相似度高达 99.73%(系统发育树分析结果见附录 1)。据此, 初步鉴定该菌株为科贝特氏菌属, 并命名为 Cobetia sp. 29。
全基因组序列分析表明, Cobetia sp. 29 的基因组总长度为 4136490bp, GC 含量为 62.48%。共预测3454 个编码基因, 总长度为 3447930bp, 平均长度为 998bp, 占全基因组的 83.35%。Cobetia sp. 29 编码基因预测长度如图 2 所示, 其中 900~1000bp 的序列有 285 个, 数量最多, 占全部编码基因的 8.25%。基因区间的长度为 688560bp, 基因区间的 GC 含量为 57.22%, 基因区间占基因的百分比为 16.65%。Cobetia sp. 29 中含有 8 个基因组岛, 4 个前噬菌体, 总长度为 103866bp。另外, 菌株 Cobetia sp. 29 中还含 12 个 rRNA (5S rRNA 8 个, 16S rRNA 3 个, 23S rRNA 1 个)、70 个 tRNA 和 2 个 sRNA。基于全基因组序列分析, 该菌株与 Cobetia marina strain JCM 21022 的平均核苷酸一致性(average nucleotide iden-tity, ANI)达到 95.03%, 与 16S rDNA 序列分析结果相符, 将其命名为 Cobetiamarina 29。
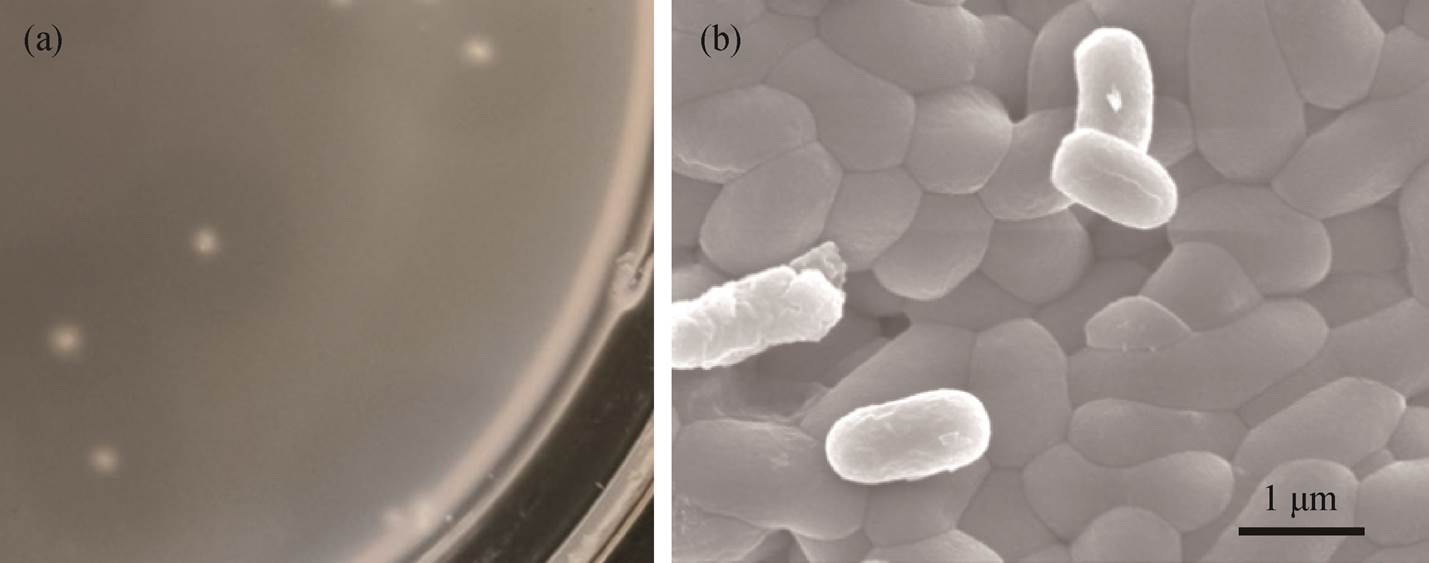
图1 菌株 Cobetia sp. 29 的菌落形态(a)和扫描电镜图像(b)
Fig. 1 Colony morphology (a) and SEM image (b) of strain Cobetia sp. 29
表4 菌株 Cobetia sp. 29 的生理生化特性
Table 4 Physiological and biochemical characteristics of strain Cobetia sp. 29

试验项目反应结果试验项目反应结果 葡萄糖+5% NaCl+ 蔗糖+20°C+ 乳糖−30°C+ 木糖−37°C+ 淀粉−甲基红− 0% NaCl+淀粉水解− 2.5% NaCl+明胶液化+
说明: +为阳性反应, −为阴性反应。
为深入探究菌株 Cobetia marina 29 的功能, 对编码基因进行基因本体(Gene Ontology, GO)、京都基因与基因组百科全书(Kyoto Encyclopedia of Ge-nes and Genomes, KEGG)、同源基因簇(Clusters of Orthologous Groups of Proteins, COG)及碳水化合物活性酶(Carbohydrate-Active EnZymes, CAZy)数据库的功能注释分析。结果显示, GO 数据库中成功注释 2487 个基因, 占总基因数的 71.97%; KEGG 数据库中注释 2271 个基因, 占 65.75%; COG 数据库中注释 2910 个基因, 占 84.25%; CAZy 数据库中注释 145个基因, 占 4.20%。
2.3.1 GO注释分析
Cobetiamarina 29 在 GO 数据库中的注释结果如图 3 所示。在分子功能(molecular function)方面有10 个分类, 其中以催化活性(catalytic activity)为主, 占 45.80%。在细胞组分(cellular component)方面有5 个分类, 主要是细胞内结构(cellular anatomical entity), 占 68.57%。在生物过程(biological process)方面有 19 个分类, 代谢过程(metabolic process)是关键功能, 占 30.44%。总体而言, Cobetiamarina 29 在分子层面以催化活性和结合功能为主, 在细胞结构上以内部分布为主, 在生物学过程中则以代谢和细胞活动为核心。
2.3.2 KEGG 与 COG 注释分析
菌株 Cobetia marina 29 的 KEGG 代谢途径基因注释结果如图 4 所示。细胞过程(cellular proces-ses)、环境信息处理(environmental information pro-cessing)、遗传信息处理(genetic information proces-sing)、人类疾病(human diseases)、代谢(metabo-lism)和生物系统(organismal systems)相关通路基 因分别占基因组的 8.79%, 14.94%, 9.13%, 6.25%, 58.30%和 2.59%。在代谢相关途径中, 氨基酸代谢(amino acid metabolism)途径基因数占比最大, 为21.02%; 碳水化合物代谢(carbohydrate metabolism)途径基因数占比次之, 为 11.59%。
菌株 Cobetiamarina 29 基因组注释的蛋白质序列在 COG 数据库比对分析结果如图 5 所示。其中, 功能基因注释最丰富的两类分别是氨基酸的转运与代谢(amino acid transport and metabolism)基因(共354 个), 以及转录(transcription)基因(共 239 个), 分别占注释基因的 10.95%和 7.39%。进一步分析参与碳水化合物运输和代谢的特定 COG, 结果显示该菌株中共有 212 个基因被注释为参与碳水化合物运输与代谢。为了更好地了解菌株 Cobetiamarina 29降解褐藻胶的代谢通路, 我们分析了褐藻胶多糖利用位点(AULs)包含的关键酶基因。结果显示, 其中有3 个褐藻胶裂解酶(alys)基因, 特异性地断裂褐藻 胶中的 β-1,4-糖苷键, 从而将其降解为低分子量的寡糖。我们还发现几个关键酶基因, 包括一个 kdgF(果胶降解蛋白)基因, 能够将单糖转化为 4-脱氧-L-赤型-5-己糖糖醛酸; 一个 kdgK (2-脱氢-3-脱氧葡萄糖酸激酶)基因和 3 个 eda基因(KDG-6-磷酸醛缩酶), 能够将 2-酮-3-脱氧葡萄糖酸降解为丙酮酸和甘油醛-3-磷酸[39–40]。此外, 还注释到 3 个与磷酸转移酶系统相关的基因(参与多种单糖、二糖、多元醇和其他糖衍生物的转运和磷酸化[41])、23 个溶质结合蛋白基因(负责将藻酸盐传递给 ABC 转运蛋白)以及 3 个与碳水化合物吸收相关的 ABC 型糖转运体[42](能够跨膜运输藻酸盐)。上述结果不仅暗示该菌在褐藻胶的代谢途径中扮演重要的角色, 也表明此菌株在降解糖类、吸收和运输糖类等方面有巨大潜力。
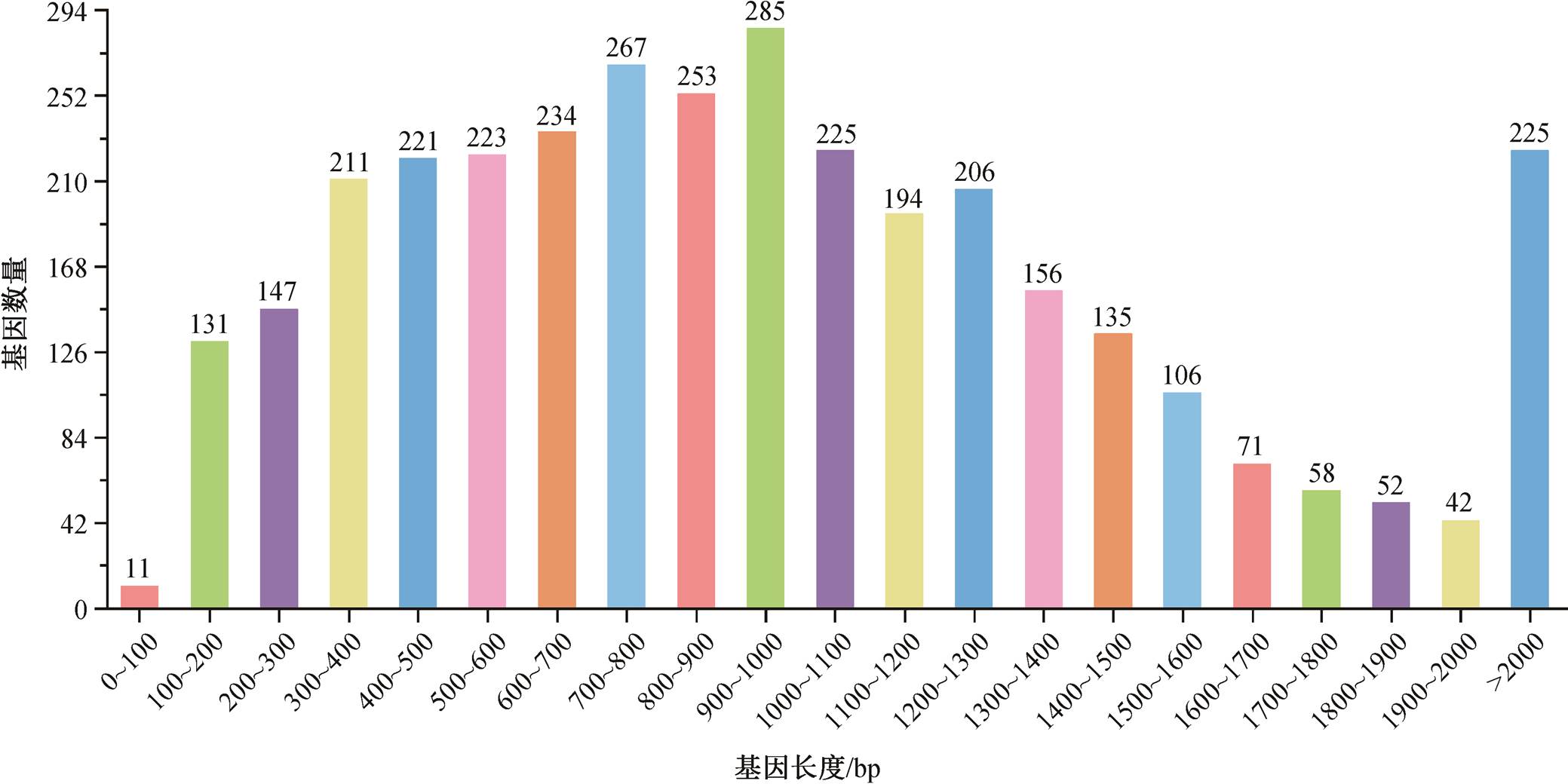
图2 菌株 Cobetia sp.29 的编码基因长度
Fig. 2 Length map of genes encoded by strain Cobetia sp. 29

图3 GO 注释分析结果
Fig. 3 GO annotation analysis

图4 KEGG 注释分析结果
Fig. 4 KEGG annotation analysis
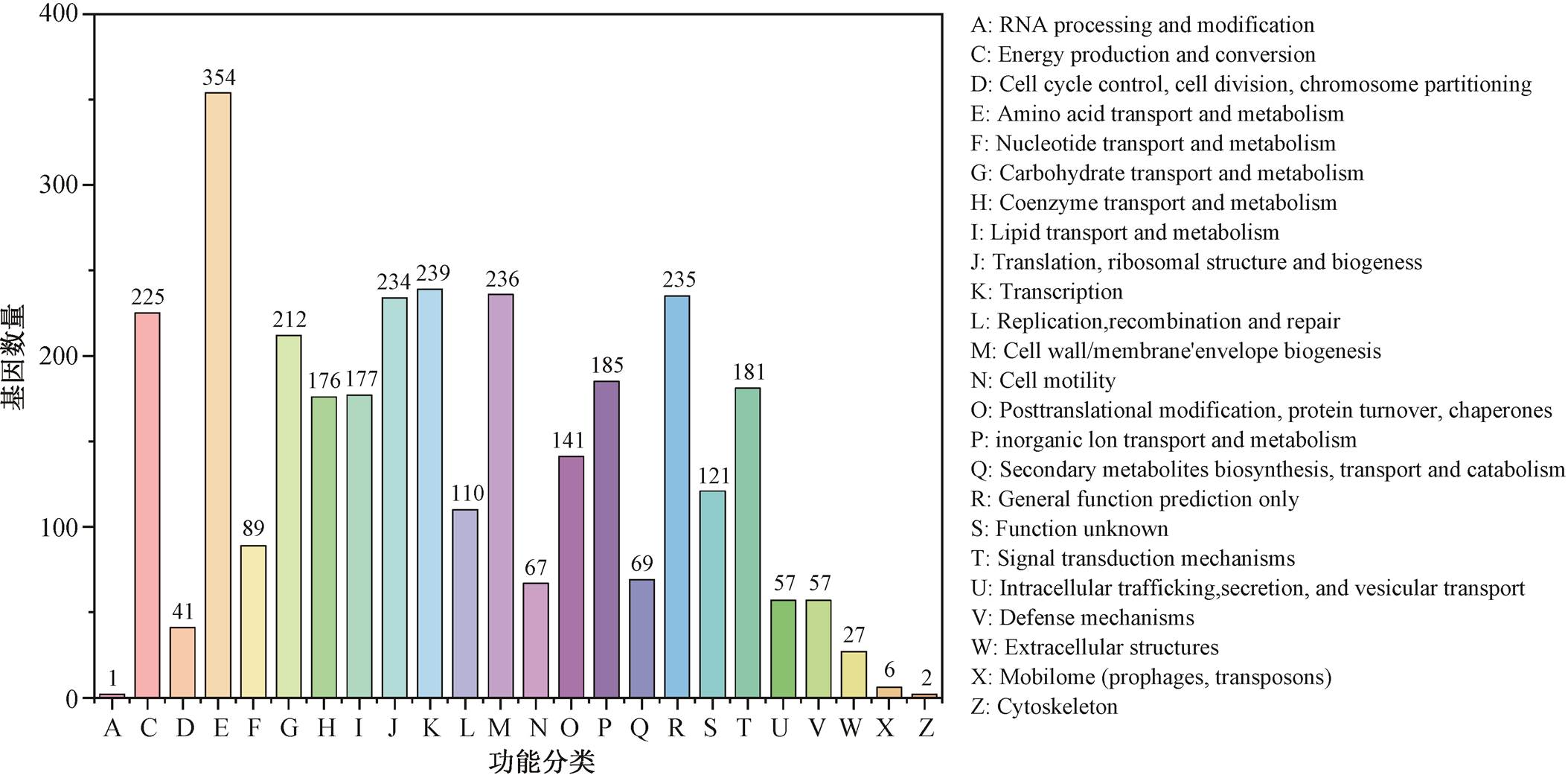
图5 COG 注释分析结果
Fig. 5 COG annotation analysis
2.3.3 CAZy富集分析
碳水化合物活性酶在微生物代谢中扮演着至关重要的角色, 它们不仅负责生物体内所有糖类的生物合成、修饰和降解, 在维持宿主健康和疾病预防方面也发挥重要作用[43]。CAZy 数据库注释结果如图 6 所示, 菌株 Cobetia marina 29 共注释到 145 个基因。其中, 氧化还原酶(AA)、碳水化合物结合组件(CBM)、糖酯酶(CE)、糖苷水解酶(GH)、糖基转移酶(GT)和多糖裂解酶(PL)基因分别有 5, 17, 7, 42, 70 和 4 个。此外, 注释到 3 个有关褐藻胶裂解酶序列基因: alginate lyase (EC 4.2.2.3), oligoalginate lyase (EC 4.2.2.26)和 alpha-L-guluronate lyase/G-specific alginate lyase (EC 4.2.2.11))[44–47]。前两种属于 PL17家族基因, 后一种属于 PL7 家族基因。NCBI 数据库比对结果显示, PL17 家族的两种褐藻胶裂解酶基因序列分别与 Halomonas sp. QY114 产的褐藻裂解酶基因(KU598831.1)[38]以及 Cobetia marina strain KMM 1449 产的褐藻裂解酶基因(CP173426.1)的序列相似度高达 99.44%和 99.11%, 推测两者可能是特异性降解 PM 的外切褐藻胶裂解酶, 酶解产物主要为单糖和(或)二糖[48]。PL7 家族的褐藻胶裂解酶基因与 Cobetia marina strain JCM 21022 (CP017114.1)的相似度为 99.23%, 推测其可能是可以降解 PM 和PG 的双功能内切褐藻胶裂解酶, 酶解产物主要为二糖和三糖[49]。结构分析表明, 这些基因编码蛋白质都包含相同的保守结构域。总之, 该菌株在褐藻胶降解方面具有一定的遗传基础和应用潜力。
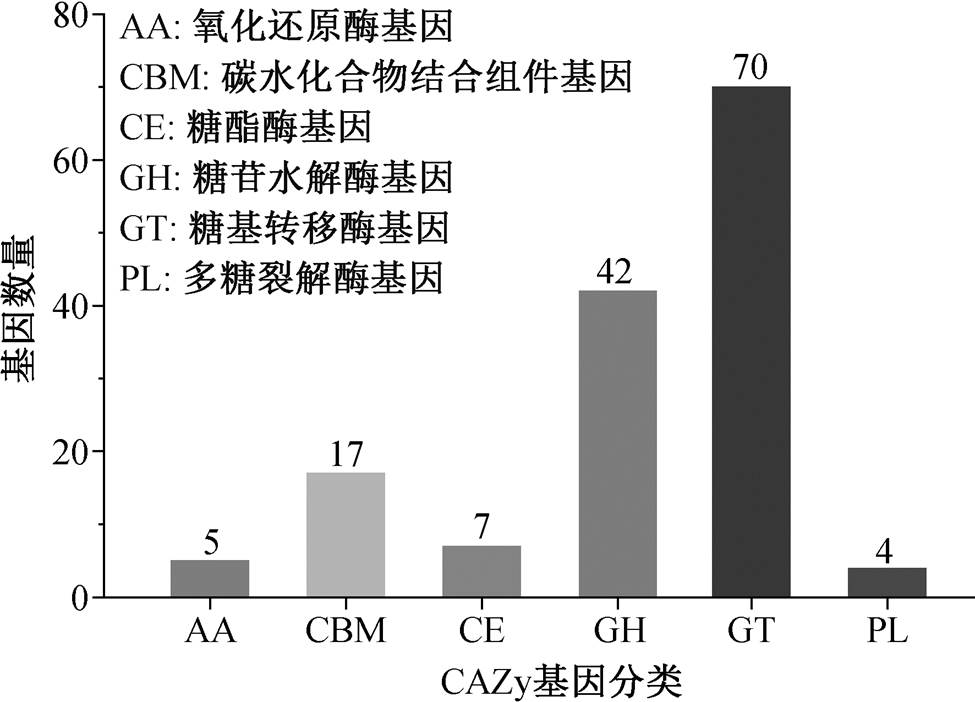
图6 CAZy 注释分析结果
Fig 6 CAZy annotation analysis
基因组分析揭示了 Cobetia marina 29 的遗传背景, 特别是在其基因组中发现多个编码褐藻胶裂解酶的基因。为进一步明确该菌株的产酶能力, 对其进行发酵条件优化, 以便在工业化生产中更高效地利用 Cobetia marina 29 产生的褐藻胶裂解酶, 提高生物转化过程的效率和经济效益。
2.4.1 单因素试验
1)不同碳源对产酶的影响。培养基中碳源的类型可能会影响细菌细胞的结构, 从而影响其产酶效率。如图 7(a)所示, 当褐藻胶作为唯一碳源时, Cobetia marina 29 的酶活性最高; 其次是麦芽糖作为唯一碳源, 酶活性较高; 而以淀粉、葡萄糖为碳源时, 酶活性显著降低。这一现象与已报道的产褐藻胶裂解酶的菌株 QY102[50]相似, 表明褐藻胶对于诱导产酶是必要的。因此, 后续试验中采用褐藻胶作为培养基的唯一碳源。
2)褐藻胶浓度对产酶的影响。如图 7(b)所示, 随着褐藻胶浓度从 5g/L 增至 15g/L, 酶活性增强, 15g/L 时达到峰值。随后, 浓度继续增加至 20g/L, 酶活性降低; 在 20~30g/L 范围内, 酶活性趋于稳定并呈现下降趋势。这表明, 褐藻胶浓度较低时, 可能由于营养不足导致酶产生能力下降, 浓度过高则可能导致培养基黏稠度增加, 不利于菌体酶的分泌[51]。因此, 15g/L 的褐藻胶浓度为最佳实验标准。
3)不同氮源对产酶的影响。菌株 Cobetiamari-na 29 展现出对多种氮源的利用能力, 但其对各类氮源的利用效率存在差异。研究表明, 不同微生物对氮源的偏好各不相同, 例如中华黄海杆菌 QM42偏好蛋白胨[52], 大西洋假交替单胞菌 AR06 则偏好硝酸铵[53]。如图 7(c)所示, Cobetia marina 29 在以硫酸铵为唯一氮源时, 能够达到最高的酶活性; 以氯化铵为氮源时, 酶活性约为最高值的 59.3%; 以牛肉膏、酵母浸粉和蛋白胨为氮源时, 酶活性分别为最高值的 59.3%, 8.5%, 7.4%和 7.3%。因此, 后续实验将以硫酸铵作为培养基中的氮源。
4)硫酸铵浓度对产酶的影响。如图 7(d)所示, 当硫酸铵的浓度在 2.5~7.5g/L 范围内时, 菌株 Cobe-tiamarina 29 产酶的酶活性显著提高, 在 7.5g/L 时达到峰值; 当增加至 7.5~12.5g/L 时, 酶活性下降。氮源的不足会限制菌株的生长和代谢, 氮源的过量则可能导致代谢产物的积累, 进而影响酶的产生[54]。因此, 后续实验中硫酸铵的浓度设定为 7.5g/L。
5)氯化钠浓度对产酶的影响。如图 7(e)所示, 在 5~15g/L 的范围内, 随着氯化钠浓度增加, Cobe-tiamarina 29 菌株的酶活性提高, 在 15g/L 时达到最大值; 当浓度继续增至 15~30g/L 时, 酶活性逐渐下降。这一现象反映出氯化钠对海洋来源菌株生长的重要性, 这是海洋微生物的一个典型特征[55], 与Shewanella sp. YH1[56]和 Vibrio sp. QY108[57]对氯化钠的需求相似。因此, 后续实验中将氯化钠的浓度定为 15g/L。
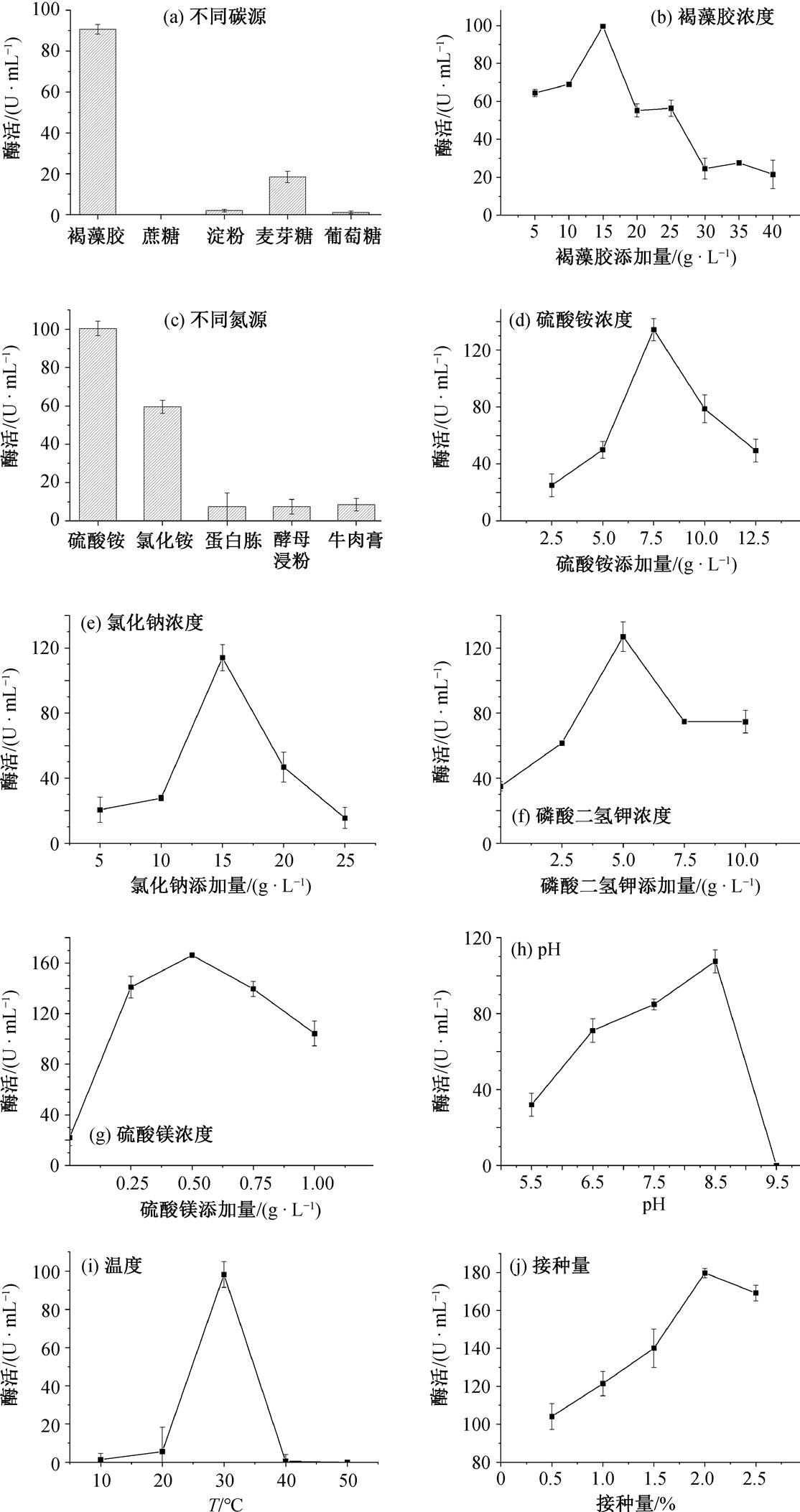
图7 各因素产酶条件的优化
Fig. 7 Optimization of enzyme production conditions for different factors
6)磷酸二氢钾浓度对产酶的影响。海洋细菌的生长与酶的产生受无机盐浓度影响。由图 7(f)可知, 磷酸二氢钾浓度在 0~5.0g/L 范围内时, 菌株产酶的酶活性呈现上升趋势, 在 5.0g/L 时达到最高; 浓度在 5.0~10.0g/L 时, 酶活性呈下降趋势。可能是磷酸二氢钾浓度过大导致培养基的 pH 降低, 不利于菌株生长[58]。因此, 选择磷酸二氢钾的浓度为5.0g/L 作为后续实验的基础。
7)硫酸镁浓度对产酶的影响。如图 7(g)所示, 硫酸镁浓度在 0~0.5g/L 范围内时, 菌株产酶的酶活性逐渐升高, 并在 0.5g/L 时达到峰值; 在 0.5~1.0g/L 时酶活性下降。因此, 选择硫酸镁浓度为 0.5g/L 进行后续试验。
8) pH 值对产酶的影响。如图 7(h)所示, 菌株产酶的酶活性随着 pH 值的增加呈现先上升后下降的趋势。在 pH 值为 8.5 时, 酶活性达到峰值, 当 pH 值继续增加时, 酶活性降低, 直至降至零。这一最适 pH 值与刘彩琴等[59]报道的褐藻胶裂解酶的最适pH 值吻合。由此, 选择 pH 值为 8.5 的培养基发酵 条件。
9)温度对产酶的影响。温度是影响微生物生长及其代谢功能的关键因素。由图 7(i)可知, 当温度为 10~30°C 时, Cobetiamarina 29 菌株的酶活力随温度升高而增强; 超过 30°C, 酶活性急剧下降; 在40°C 以上时, 酶活力几乎消失。因此, Cobetiamari-na 29 菌株产酶的最佳温度为 30°C。这一结果与现有研究一致, 即大多数褐藻胶降解菌的产酶最适温度为 25~30°C[24]。
10)接种量对产酶的影响。图 7(j)显示接种量对 Cobetiamarina 29 产酶效果的影响。随着接种量从 0.5%升至 2.0%, 酶活性逐渐提升, 并在接种量达到 2.0%时达到最高。继续增加接种量至 2.5%时, 酶活性降低。因此, 2.0%的接种量是最佳选择。
2.4.2 Plackett-Burman试验分析
根据单因素试验的结果, 试验设计见表5, 数据分析见附录 2。显著性从低到高为褐藻胶、氯化钠、硫酸镁、磷酸二氢钾、接种量、硫酸铵、pH和温度。其中, 温度、pH 和硫酸铵对酶活的影响显著(P<0.05)。如图 8 所示, 超过参考线的硫酸铵(A)、pH (B)和温度(C)3 个因素对酶活性影响显著。
2.4.3 响应面试验分析
用 Design-Expert 软件设计响应面试验, 并建立回归模型, 实验方案如表6 所示, 结果分析如表7所示。响应面方程为 Y=178.27−3.42A − 12.29B − 7.99 + 9.27AB − 21.46AC − 23.74BC − 24.38A2 − 50.34B2 − 47.23C2。
由表6 可知, 模型的统计分析结果揭示变量AC, BC, A2, B2和 C2对酶活性有显著影响(P<0.01), 变量 B和 C也影响显著(P<0.05), 试验拟合性良好。模型失拟项 P=8.70>0.05, 决定系数 R2=0.9863, 信噪比=6.51>4.0, 表明实验数据与模型间匹配度高, 有较高的可靠性, 能有效地对实验响应值进行分析和预测。
Design-Expert 软件对数据拟合结果如图 9 所示。三维曲面的两端向下弯曲的形状暗示酶活性存在一个最优值, 曲面斜率的急剧变化显示各因素间相互作用的程度, 其中 AB因素的相互作用最为显著, 其次是 AC, 最后是 BC。通过软件分析和优化, 确定Cobetiamarina 29 产酶培养基的最优条件: 硫酸铵浓度为 7.39g/L, pH 为 7.94, 温度为 29.81°C。考虑到试验方案的可行性, 调整为硫酸铵浓度=7.39g/L, pH=7.94, 温度=30°C。通过 5 组试验进行验证, 酶活力的平均值为 179.29U/mL, 相较于优化前的测定值提高 53.6%。与 Cobetia marina HQZ08(68.5U/ mL)[24]相比, 经优化后菌株 Cobetiamarina 29 的产酶活力更高。
表5 Plackett-Burman 试验因素组合及酶活响应结果
Table 5 Factor combinations and enzyme activity results of Plackett-Burman experiment
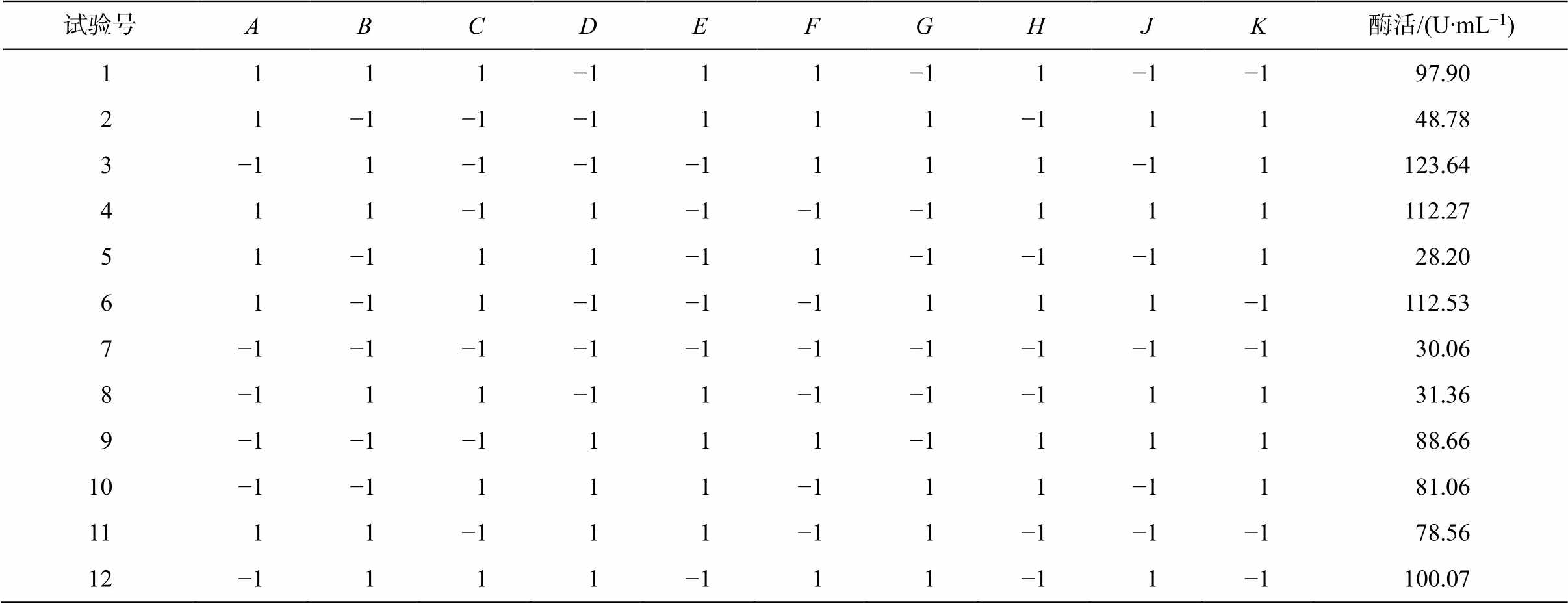
试验号ABCDEFGHJK酶活/(U∙mL−1) 1111−111−11−1−197.90 21−1−1−1111−11148.78 3−11−1−1−1111−11123.64 411−11−1−1−1111112.27 51−111−11−1−1−1128.20 61−11−1−1−1111−1112.53 7−1−1−1−1−1−1−1−1−1−130.06 8−111−11−1−1−11131.36 9−1−1−1111−111188.66 10−1−1111−111−1181.06 1111−111−11−1−1−178.56 12−1111−111−11−1100.07
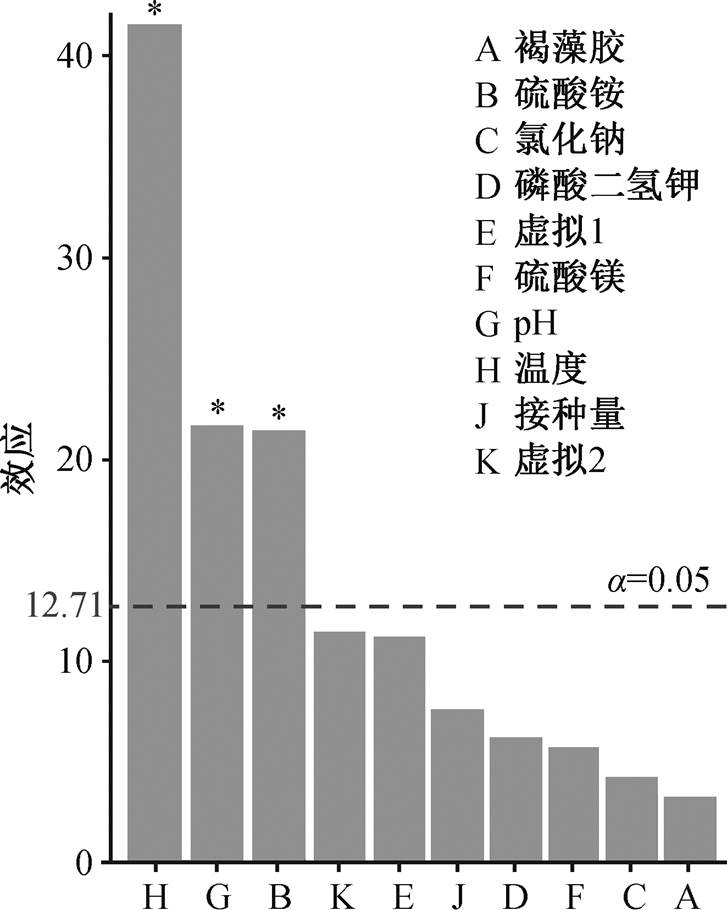
图8 因素影响柏拉图
Fig. 8 Pareto chart of factor effects
本研究以海藻为实验材料, 经筛选获得一株高效降解褐藻胶的细菌菌株 29。通过形态学、生理生化特征、16S rDNA 序列分析以及基因组平均核苷酸一致性比对分析, 鉴定该菌株为海科贝特氏菌, 并将其命名为 Cobetia marina 29。全基因测序结果显示, 菌株 Cobetia marina 29 具有丰富的降解糖类、吸收和运输糖类等方面的功能基因, 并注释到3 个有关褐藻胶裂解酶基因序列, 揭示该菌株在褐藻胶降解方面具有一定的遗传基础和应用潜力。本研究采用单因素产酶优化、Plackett-Burman 试验以及响应面试验法对 Cobetia marina 29 进行优化, 优化后的酶活力提升至 179.29U/mL, 比优化前提高53.6%。本文研究结果不仅丰富了微生物资源库, 可为褐藻胶的生物降解提供新的生物催化剂, 也为工业化生产褐藻胶裂解酶奠定基础。
表6 响应面试验因素组合及酶活响应结果
Table 6 Factor combinations and enzyme activity results of response surface experiment
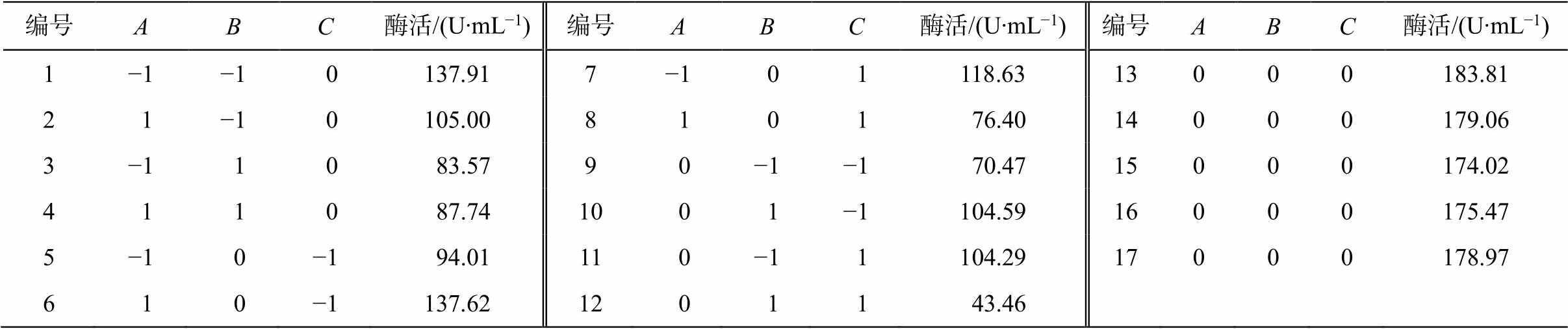
编号ABC酶活/(U∙mL−1)编号ABC酶活/(U∙mL−1)编号ABC酶活/(U∙mL−1) 1−1−1 0137.917−1 0 1118.6313000183.81 2 1−1 0105.008 1 0 1 76.4014000179.06 3−1 1 0 83.579 0−1−1 70.4715000174.02 4 1 1 0 87.7410 0 1−1104.5916000175.47 5−1 0−1 94.0111 0−1 1104.2917000178.97 6 1 0−1137.6212 0 1 1 43.46
表7 响应面回归模型方差分析
Table 7 Analysis of variance for response surface regression model
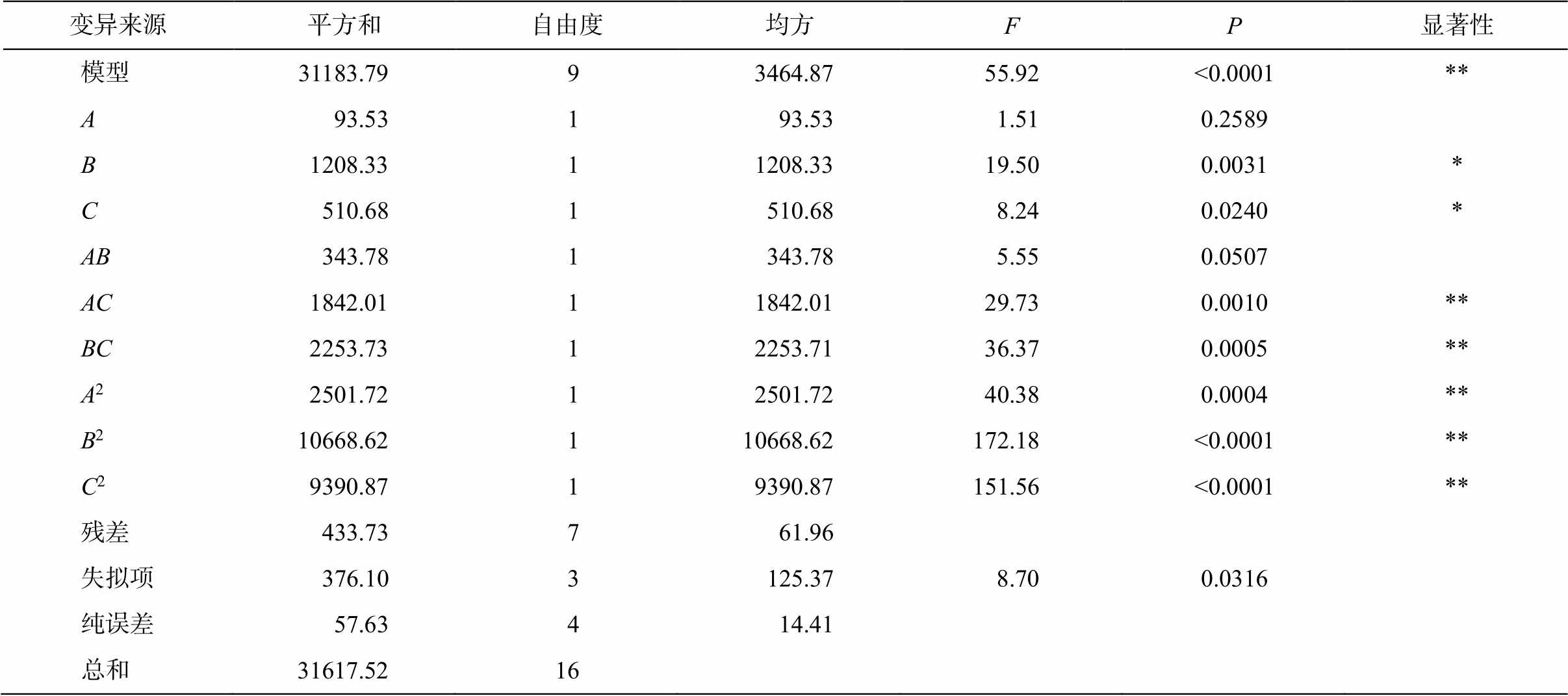
变异来源平方和自由度均方FP显著性 模型31183.79 93464.8755.92<0.0001** A93.53 193.531.510.2589 B1208.33 11208.3319.500.0031* C510.68 1510.688.240.0240* AB343.78 1343.785.550.0507 AC1842.01 11842.0129.730.0010** BC2253.73 12253.7136.370.0005** A22501.72 12501.7240.380.0004** B210668.62 110668.62172.18<0.0001** C29390.87 19390.87151.56<0.0001** 残差433.73 761.96 失拟项376.10 3125.378.700.0316 纯误差57.63 414.41 总和31617.5216
注: *表示P<0.05; **表示P<0.01。
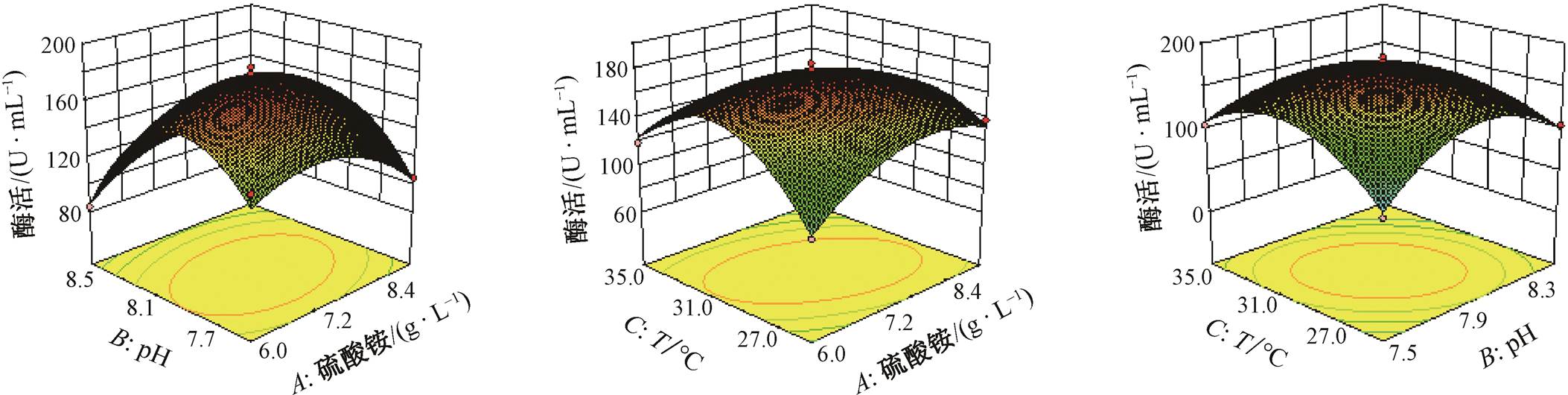
图9 硫酸铵、pH 和温度交互作用对酶活影响的响应面
Fig. 9 Response surface diagram of the interaction between ammonium sulfate, pH, and temperature on enzyme activity
参考文献
[1] Gacesa P. Enzymic degradation of alginates. Interna-tional Journal of Biochemistry, 1992, 24(4): 545–552
[2] 陈俊帆, 石波, 范红玲, 等. 褐藻胶裂解酶的研究进展. 食品工业科技, 2011, 32(8): 428–431
[3] Hasnain M S, Jameel E, Mohanta B, et al. Alginates: sources, structure, and properties // Nayak A K, Hasnain M S. Alginates in drug delivery. London: Academic Press, 2020: 1–17
[4] Li J W, Dong S, Song J, et al. Purification and charac-terization of a bifunctional alginate lyase from Pseu-doalteromonas sp. SM0524. Marine Drugs, 2011, 9(1): 109–123
[5] Liu J, Yang S, Li X, et al. Alginate oligosaccharides: Production, biological activities, and potential applica-tions. Comprehensive Reviews in Food Science and Food Safety, 2019, 18(6): 1859–1881
[6] Khalil H P S, Lai T K, Tye Y Y, et al. A review of extractions of seaweed hydrocolloids: properties and applications. Express Polymer Letters, 2018, 12(4): 296–317
[7] Bojorges H, López-Rubio A, Martínez-Abad A, et al. Overview of alginate extraction processes: impact on alginate molecular structure and techno-functional pro-perties. Trends in Food Science & Technology, 2023, 140: 104142
[8] Chen C, Li X, Lu C, et al. Advances in alginate lyases and the potential application of enzymatic prepared alginate oligosaccharides: a mini review. International Journal of Biological Macromolecules, 2024, 260: 129506
[9] Vasudevan U M, Lee O K, Lee E Y. Alginate deri- ved functional oligosaccharides: recent developments, barriers, and future outlooks. Carbohydrate Polymers, 2021, 267: 118158
[10] 阿拉腾珠拉, 胡永飞. 褐藻寡糖的制备方法及生物活性研究进展. 生物工程学报, 2022, 38(1): 104–118
[11] Li L, Zhu B, Yao Z, et al. Directed preparation, struc-ture–activity relationship and applications of alginate oligosaccharides with specific structures: a systematic review. Food Research International, 2023, 170: 112990
[12] Kaur S, Abraham R E, Franco C M M, et al. Production of alginate oligosaccharides (AOSs) using enhanced physicochemical properties of immobilized alginate lyase for industrial application. Marine Drugs, 2024, 22(3): 120
[13] Zhu B, Li L, Yuan X. Efficient preparation of alginate oligosaccharides by using alginate lyases and evalua-tion of the development promoting effects on Brassica napus L. in saline-alkali environment. International Journal of Biological Macromolecules, 2024, 270: 131917
[14] 王海英, 陈志芳, 朱甜甜, 等. 海洋弧菌 Vibrio sp. L2褐藻胶裂解酶AlgL3199的表达及酶学性质研究. 食品与发酵工业, 2025, 51(15): 174–184
[15] Xu F, Wang P, Zhang Y Z, et al. Diversity of three-dimensional structures and catalytic mechanisms of alginate lyases. Applied and Environmental Microbio-logy, 2018, 84(3): e02040-17
[16] 李京宝, 于文功, 韩峰, 等. 从海洋中分离的弧菌QY102 褐藻胶裂解酶的纯化和性质研究. 微生物学报, 2003, 6(6): 753–757
[17] 闫军军, 陈朋, 田朝玉, 等. 海洋细菌来源的新型耐碱褐藻胶裂解酶研究//中国微生物学会酶工程专业委员会. 第十二届中国酶工程学术研讨会. 长春, 2019: 172
[18] Zhu B, Yin H. Alginate lyase: review of major sources and classification, properties, structure-function analy-sis and applications. Bioengineered, 2015, 6(3): 125–131
[19] Ertesvåg H. Alginate-modifying enzymes: biological roles and biotechnological uses. Frontiers in Micro-biology, 2015, 6: 523
[20] Gimmestad M, Ertesvåg H, Heggeset T M B, et al. Characterization of three new Azotobacter vinelandii alginate lyases, one of which is involved in cyst ger-mination. Journal of Bacteriology, 2009, 191: 4845–4853
[21] Preston L A, Wong T Y, Bender C L, et al. Characteri-zation of Alginate Lyase from Pseudomonas syringae pv. syringae. Journal of Bacteriology, 2000, 182: 6268–6271
[22] Linker A. Isolation and characterization of an alginase from mucoid strains of Pseudomonasaeruginosa. Jour-nal of Bacteriology, 1984, 159: 958–964
[23] 李丽妍, 管华诗, 江晓路, 等. 海藻工具酶——褐藻胶裂解酶研究进展. 生物工程学报, 2011, 27(6): 838–845
[24] 赵婉琳, 叶静, 张娜, 等. 褐藻胶降解菌的筛选、鉴定及产酶条件优化. 微生物学报, 2019, 59(1): 169–180
[25] Ratnayake K, Joyce D C, Webb R I. A convenient sam-ple preparation protocol for scanning electron micros-cope examination of xylem-occluding bacterial bio-film on cut flowers and foliage. Scientia Horticulturae, 2012, 140: 12–18
[26] 东秀珠, 蔡妙英. 常见细菌系统鉴定手册. 北京: 科学出版社, 2001: 353–398
[27] Baker G C, Smith J J, Cowan D A. Review and re-analysis of domain-specific 16S primers. Journal of Microbiological Methods, 2003, 55(3): 541–555
[28] Hogg J C, Lehane M J. Identification of bacterial spe-cies associated with the sheep scab mite (Psoroptes ovis) by using amplified genes coding for 16S rRNA. Applied and Environmental Microbiology, 1999, 65 (9): 4227–4229
[29] Li R, Li Y, Kristiansen K, et al. SOAP: short oligonuc-leotide alignment program. Bioinformatics, 2008, 24 (5): 713–714
[30] Bankevich A, Nurk S, Antipov D, et al. SPAdes: a new genome assembly algorithm and its applications to single-cell sequencing. Journal of Computational Bio-logy, 2012, 19(5): 455–477
[31] Simpson J T, Wong K, Jackman S D, et al. ABySS: a parallel assembler for short read sequence data. Ge-nome Research, 2009, 19(6): 1117–1123
[32] Lowe T M, Eddy S R. tRNAscan-SE: a program for improved detection of transfer RNA genes in genomic sequence. Nucleic Acids Research, 1997, 25(5): 955–964
[33] Hsiao W, Wan I, Jones S J, et al. IslandPath: aiding detection of genomic islands in prokaryotes. Bioinfor-matics, 2003, 19(3): 418–420
[34] Lagesen K, Hallin P, Rødland E A, et al. RNAmmer: consistent and rapid annotation of ribosomal RNA ge-nes. Nucleic Acids Research, 2007, 35(9): 3100–3108
[35] 潘琳. 利用比较蛋白质组学与代谢组学研究 Lacto-bacillus casei Zhang 在葡萄糖限制性环境中的生长代谢规律[D]. 呼和浩特: 内蒙古农业大学, 2019
[36] 成珍. 多糖降解菌的筛选鉴定及培养条件优化——褐藻胶和菊芋降解菌的分离纯化[D]. 青岛: 青岛科技大学, 2014
[37] 宋鑫, 秦送玉, 朱军, 等. 产褐藻胶裂解酶海洋细菌的筛选和鉴定. 基因组学与应用生物学, 2016, 35 (4): 907–912
[38] Arahal D R, Castillo A M, Ludwig W, et al. Proposal of Cobetia marina gen. nov., comb. nov., within the family Halomonadaceae, to include the species Halo-monas marina. Systematic and Applied Microbiology, 2002, 25(2): 207–211
[39] Hobbs J K, Lee S M, Robb M, et al. KdgF, the missing link in the microbial metabolism of uronate sugars from pectin and alginate. Proceedings of the National Academy of Sciences, 2016, 113(22): 6188–6193
[40] Wargacki A J, Leonard E, Win M N, et al. An engi-neered microbial platform for direct biofuel production from brown macroalgae. Science, 335: 308–313
[41] Wang C, Dong D, Wang H, et al. Metagenomic analysis of microbial consortia enriched from compost: new insights into the role of Actinobacteria in lignocellu-lose decomposition. Biotechnology for Biofuels, 2016, 9: 1–17
[42] Nanavati D M, Thirangoon K, Noll K M. Several ar-chaeal homologs of putative oligopeptide-binding pro-teins encoded by Thermotoga maritima bind sugars. Applied and Environmental Microbiology, 2006, 72(2): 1336–1345
[43] Bains R K, Nasseri S A, Wardman J F, et al. Advances in the understanding and exploitation of carbohydrate-active enzymes. Current Opinion in Chemical Biology, 2024, 80: 102457
[44] Kim H T, Ko H J, Kim N, et al. Characterization of a recombinant endo-type alginate lyase (Alg7D) from Saccharophagus degradans. Biotechnology Letters, 2012, 34: 1087–1092
[45] Kim H T, Chung J H, Wang D, et al. Depolymerization of alginate into a monomeric sugar acid using Alg17C, an exo-oligoalginate lyase cloned from Saccharopha-gus degradans 2-40. Applied Microbiology and Biote-chnology, 2012, 93: 2233–2239
[46] Park H H, Kam N, Lee E Y, et al. Cloning and charac-terization of a novel oligoalginate lyase from a newly isolated bacterium Sphingomonas sp. MJ-3. Marine Biotechnology, 2012, 14: 189–202
[47] Jagtap S S, Hehemann J H, Polz M F, et al. Compara-tive biochemical characterization of three exolytic oli-goalginate lyases from Vibrio splendidus reveals com-plementary substrate scope, temperature, and pH adap-tations. Applied and Environmental Microbiology, 2014, 80(14): 4207–4214
[48] 薛钊. 马尾藻附生褐藻胶降解菌的分离、褐藻胶代谢通路分析及新型褐藻胶裂解酶的挖掘[D]. 济南: 山东师范大学, 2022
[49] Mathieu S, Touvrey-Loiodice M, Poulet L, et al. Anci-ent acquisition of “alginate utilization loci” by human gut microbiota. Scientific Reports, 2018, 8(1): 8075
[50] 傅晓妍, 李京宝, 韩峰, 等. 褐藻胶裂解酶产生菌Vibro sp. QY102的发酵条件优化. 中国海洋大学学报(自然科学版), 2007, 37(3): 432–436
[51] Zhu Y, Wu L, Chen Y, et al. Characterization of an extracellular biofunctional alginate lyase from ma-rine Microbulbifer sp. ALW1 and antioxidant activity of enzymatic hydrolysates. Microbiological Research, 2016, 182: 49–58
[52] 王霁宁, 严孝强, 杜宗军. 一株高效褐藻胶降解菌的筛选及其发酵条件的优化. 中国酿造, 2012, 31 (5): 7–10
[53] Matsushima R, Watanabe R, Tsuda M, et al. Analysis of extracellular alginate lyase (alyA) expression and its regulatory region in a marine bacterial strain, Pseudo-alteromonas atlantica AR06, using a gfp gene reporter system. Marine Biotechnology, 2013, 15(3): 349–356
[54] 李梦. 褐藻胶降解菌产酶条件优化及酶解产物分析[D]. 烟台: 烟台大学, 2024
[55] 吴阳. 褐藻胶裂解酶产生菌 BY-1 的筛选、培养及酶学性质研究[D]. 烟台: 烟台大学, 2021
[56] Yagi H, Fujise A, Itabashi N, et al. Characterization of a novel endo-type alginate lyase derived from She-wanella sp. YH1. The Journal of Biochemistry, 2018, 163(4): 341–350
[57] Zhang F, Fu Z, Tang L, et al. Biochemical characteri-zation of a novel exo-type PL7 alginate lyase VsAly7D from marine Vibrio sp. QY108. International Journal of Molecular Sciences, 2021, 22(16): 8402
[58] 张朝正, 李意, 赵华. 响应面法优化壳聚糖酶发酵培养基. 中国酿造, 2022, 41(1): 197–203
[59] 刘彩琴, 王楠, 陈薇青, 等. 一株明亮发光杆菌产褐藻胶裂解酶的培养基优化. 食品工业科技, 2017, 38(8): 156–160
附录
请访问《北京大学学报(自然科学版)》官方网站(https://xbna.pku.edu.cn)查看

Screening, Whole Genome Analysis, and Enzyme Production Optimization of Alginate Lyase-Producing Strain Cobetiamarina 29
Abstract This study successfully isolated and screened a microbial strain with efficient alginate-degrading capa-bility from seaweed, utilizing alginate as the sole carbon source in a selective culture medium. The strain was sys-tematically identified and subjected to bioinformatics analysis through physiological and biochemical characteriza-tion, 16S rDNA sequence analysis, and whole-genome sequencing to uncover potential alginate lyase-related genes. Additionally, the enzyme production conditions for the strain were optimized using single-factor experiments, Plackett-Burman design, and response surface methodology. Morphological observations, physiological and bioche-mical trait analysis, and 16S rDNA gene sequence identification confirmed the strain to be of the genus Cobetia. The full length of the strain’s genome is 4136490 base pairs, with a GC content of 62.48%. Genome prediction encoded 3454 protein-coding genes, 70 tRNA genes, and 12 rRNA genes. Nucleotide consistency analysis was subsequently performed and it was named Cobetia marina 29. Nucleotide consistency analysis was subsequently performed and it was named Cobetia marina 29. Functional annotation using the GO, KEGG, COG, and CAZy databases yielded 2487, 2271, 2910, and 145 annotated functional genes, respectively. Among these, three genes encoded alginate lyases and were classified into the PL17 and PL7 families. Finally, the cultivation parameters were refined, and under the optimal conditions for enzyme production, the enzyme activity was enhanced to 179.29 U/mL, which represented a 53.6% increase compared with the levels prior to optimization. The findings of this study provided a new microbial resource for the biodegradation of alginate and laid the foundation for subsequent industrial applications.
Key words alginate lyase; strain screening; whole genome analysis; enzyme production optimization
国家自然科学基金(31771907)和辽宁省高校基本科研项目(LJ212510152015)资助
收稿日期: 2024–10–08;
修回日期: 2025–04–14