文章信息
- 蔡斌, 王婷
- CAI Bin, WANG Ting
- 钛酸纳米管形成过程中不同水热反应阶段产物表征及其对Cd (Ⅱ)吸附的特性研究
- Characterization of Titanate Products with Different Formation Stages and Adsorption Characteristics of Cd (Ⅱ)
- 北京大学学报(自然科学版), 2016, 52(6): 1141-1147
- Acta Scientiarum Naturalium Universitatis Pekinensis, 2016, 52(6): 1141-1147
-
文章历史
- 收稿日期: 2015-05-26
- 修回日期: 2015-06-02
- 网络出版日期: 2016-11-05
2. 北京大学环境工程系, 水沙教育部重点实验室, 北京 100871
2. Department of Environmental Engineering, Peking University, The Key Laboratory of Water and Sediment Sciences, Ministry of Education, Beijing 100871
钛酸纳米管作为一种新型的纳米材料, 具有制备方法简单、管径均一、比表面积和孔体积较大、表面带电性、离子交换能力强等优点, 在重金属吸附领域有较大的研究价值与应用潜力[1]。
Kasuga等[2-3]以锐钛矿(TiO2)为钛源, 首次通过水热反应制备出钛酸纳米管。在110 C条件下, 水热反应20小时, 得到的钛酸纳米管外径为8 nm, 长100 nm, 比表面积高达400 m2/g。Chen等[4]在此基础上进行更加深入的研究, 发现在130 C、72小时条件下, 水热反应得到的钛酸纳米管为多壁结构, 层间距为0.78 nm, 外径为9 nm, 管长为100 nm至数百纳米不等。对其进行成分分析发现, 钛酸纳米管化学组成为(H, Na)2Ti3O7·xH2O, 组成纳米管的最小单元是H2Ti3O7的单斜晶形, 晶胞参数为a=1.603 nm, b=0.375 nm, c=0.919 nm, β=101.45 。Wang等[5]用P25与10 mol/L的NaOH溶液也制得吸附性能良好的钛酸纳米管。Yao等[6]采用TEM表征, 发现水热法合成的钛酸纳米管是末端开口的多壁结构, 与多壁碳纳米管不同, 钛酸纳米管的管壁不是无缝结构。TiO2原料在高浓度碱液中以单层TiO2薄片的形式剥离下来, 进一步卷曲形成钛酸纳米管。
钛酸纳米管表面具有大量可交换的羟基基团, 并且其零电荷点(point of zero charge, PZC)较低, pH > pHPZC时, 其表面带负电, 可通过离子交换和静电引力有效地吸附溶液中的阳离子。由于其较大的吸附速度与较强的吸附能力, 钛酸纳米管越来越多地用作吸附剂, 以去除废水中的Pb2+, Cd2+, Cu2+, Cr3+等离子。但是, 已有的研究大多关注金属离子的单一[5, 7-11]或者竞争吸附[10]以及吸附机理的阐述, 少有研究从钛酸纳米管形貌结构上揭示影响吸附能力的关键因素。
本文以P25二氧化钛为原料, 在钛酸纳米管(titanate nanotubes, TNTs)水热反应过程中制备一系列过程产物, 并对其进行XRD, SAXS和N2吸附/脱附等表征。以Cd (Ⅱ)为代表污染物, 研究其吸附行为。研究结果对于深入揭示影响TNTs吸附能力的关键因素, 优化TNTs的合成条件有重要意义。
1 材料与方法 1.1 不同水热时间TNTs的制备及表征将1.20 g P25 TiO2和29.04 g NaOH固体加入66 mL去离子水中, 室温下磁力搅拌24小时后, 转移到100 mL聚四氟乙烯内衬的反应釜中, 在130 C条件下进行水热反应。生成的白色固体用去离子水洗涤至上清液为中性, 无水乙醇分散, 烘干, 研细待用。改变水热反应时间分别为1, 2, 3, 4天, 以制备TNTs不同形成阶段的产物, 分别标记为TNTs-1d, TNTs-2d, TNTs-3d, TNTs-4d。
TNTs不同阶段产物的晶型结构采用常规粉末X射线衍射(XRD, Rigaku, 日本)与X射线小角散射(SAXS)进行表征。XRD扫描范围(2θ)为10°~70°, 扫描速度为4°/min, 狭缝宽0.3 mm。SAXS扫描范围(2θ)为0.6°~20°, 扫描速度为2°/min, 狭缝宽0.15 mm。TNTs的比表面积和孔径分布采用比表面积及孔隙度分析仪(ASAP 2010, Micromeritics, 美国)进行检测。
1.2 静态吸附实验以Cd (Ⅱ)为代表污染物, 研究不同水热时间下制备的TNTs的吸附能力及影响因素。配制浓度为1000 mg/L的Cd (Ⅱ)储备液, 稀释, 待用。
在一系列100 mL的锥形瓶中, 加入50 mL初始浓度分别为10, 20, 30, 40, 60, 80, 100 mg/L的Cd (Ⅱ)溶液。用0.01 mol/L的HCl或NaOH溶液, 调节初始pH值在5~6之间。向每个锥形瓶中分别投加10.0 mg (0.2 g/L) TNTs, 在25 °C, 200 rpm下充分振荡3小时以达到吸附平衡, 进行吸附等温实验。取初始样和平衡样, 用0.45 μm水系滤膜过滤, 稀释, 用电感耦合等离子体-原子发射光谱仪(Leeman, Prodigy, 美国)测定Cd (Ⅱ)的浓度。
Cd (Ⅱ)在样品上的吸附量由下式计算得到:
| $ {Q_{\text{e}}} = \frac{{({C_0}-{C_{\text{e}}})V}}{m} $ | (1) |
式中, Qe为平衡吸附量(mg/g), C0和Ce为吸附初始和平衡时溶液中Cd (Ⅱ)的浓度(mg/L), V为溶液体积(L), m为吸附剂的质量(g)。
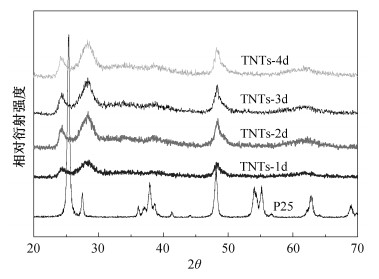
2 结果与讨论 2.1 XRD表征图 1为样品的XRD结果。可以明显看出, 在2θ=9.5°处, 除P25二氧化钛以外, 所有样品均出现明显的衍射峰, 该峰为TNTs的层间距峰[12-13]。图 1中, 位于2θ=24.32°, 28.36°和48.36°(表 1)处的峰为钛酸钠的特征峰。这表明, 参与合成反应的Na+起到稳定纳米管结构的作用[14-15]。这4个衍射峰是一种单斜晶形钛酸盐晶体的特征峰, 化学组成为(Na, H)2Ti3O7·nH2O[4]。与之相比, 二氧化钛(P25)在2θ=25.4°, 37°~39°处出现锐钛型衍射峰, 在2θ=27.5°处出现金红石型衍射峰, 这些峰在合成的样品中并没有出现, 说明在合成的TNTs阶段产物中, 无残留的二氧化钛存在。
|
| 图 1. 二氧化钛(P25)与TNTs系列样品的粉末X射线衍射谱 Figure 1. XRD patterns of various products and P25 |
| 衍射峰序号 | 2θ | θ | d/Å | h | k | l |
| 1 | 9.5 | 4.75 | 9.309 | 0 | 0 | 1 |
| 2 | 24.32 | 12.16 | 3.66 | 1 | 1 | 0 |
| 3 | 28.36 | 14.18 | 3.147 | 5 | 0 | 0 |
| 4 | 34.1 | 17.05 | 2.629 | 2 | 0 | 3 |
| 5 | 38.46 | 19.23 | 2.341 | 0 | 1 | 3 |
| 6 | 48.36 | 24.18 | 1.882 | 0 | 2 | 0 |
图 1中的衍射峰均与H2Ti3O7单斜晶形的特征峰相近或相同。已有报道也证实TiO2粉末与NaOH溶液水热反应后得到的产物为单斜晶形[16]。基于此, 表 1列出依据X射线衍射特征峰的分析结果。晶胞参数为a=1.603 nm, b=0.375 nm, c=0.919 nm, β=101.45°[4]。具体而言, 它的结构是由共用棱的TiO6八面体以类似波纹丝带的方式衔接而成。衔接时, 每3个八面体为一组[4], 每一组八面体间以顶点相互连接, 形成台阶状的分子层, 层与层之间被填充着的Na+和H+分隔开。因此, 其分子式可以简单地认为是(Na, H)2Ti3O7。
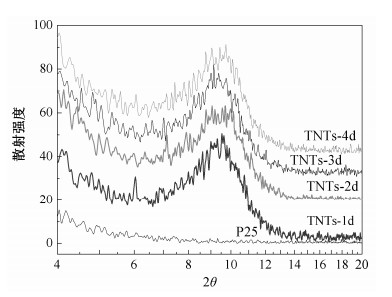
2.2 SAXS表征研究图 2为样品的SAXS结果。SAXS的结果是基于被测材料各原子中的电子对X射线的衍射和散射的叠加。被测材料中的电子密度和X射线散射测试结果中的峰值幅度之间的关系[17]如下:
| $ A(\boldsymbol{S}) = \int {\rho (\boldsymbol{r})} \;{{\text{e}}^{-{\text{i2π }}S \cdot r}}{\text{d}}\boldsymbol{r} $ | (2) |
|
| 图 2. 二氧化钛(P25)与TNTs系列样品的小角X射线散射谱 Figure 2. SAXS patterns of various products and P25 |
式中, S是入射单位矢量, 且|S|=2 sinθ/λ; r是位置矢量, 简称位矢; ρ(r)是材料在原点位置(r=0)时的电子密度。
X射线散射结果中的强度用材料中电子衍射和散射后的电磁波的振幅与它的共轭复数的乘积来计算。在形状和大小相近或相同的分散颗粒(或孔)体系中, SAXS的强度表达式[17]可简化为
| $ I(S) = I(0){{\text{e}}^{-(4{{\text{π }}^2}{S^2}{R^2})/3}} $ | (3) |
式(3)被称为Guinier公式。其中R为颗粒的回转半径, I(0)为θ=0时的衍射强度。考虑到在2θ角度较小时(2θ < 5°), S ≈ 2θ/λ, 式(3)可转换为下式[17]:
| $ I(2\theta ) = I(0){{\text{e}}^{- [4{{\text{π }}^2}{{(2\theta )}^2}{R^2}]/(3{\lambda ^2})}} $ | (4) |
取对数, 得到下式[17]:
| $ \ln [I(2\theta )] = \ln [I(0)] - [4{{\text{π }}^2}{(2\theta )^2}{R^2}]/(3{\lambda ^2}) $ | (5) |
式(5)表明, 若体系严格遵循Guinier法则, 那么ln[I(2θ)]与(2θ)2之间将线性相关。SAXS计算结果见表 2。ln[I(2q)]与r2相关系数均大于0.95, 说明体系严格遵循Guinier法则。同时, P25和TNTs阶段产物的回转半径的平方均为几百Å2, 回转半径值大多在15 Å左右, 这表明样品的介观结构可能没有任何变化。另一方面, TNTs系列样品的平均回转半径是15.85 Å, 略小于P25的16.81Å。据此可以认为, 在水热合成反应的过程中, 发生了一些结构上的转变。
| 样品名称 | 回转半径R2 /Å2 | 回转半径R/Å | 相关系数r2 |
| P25 | 282.6 | 16.81 | 0.9521 |
| TNTs-1d | 286.4 | 16.92 | 0.9656 |
| TNTs-2d | 178.3 | 13.35 | 0.9823 |
| TNTs-3d | 251.1 | 15.85 | 0.988 |
| TNTs-4d | 289.6 | 17.02 | 0.9547 |
从表 2还可以看出, TNTs-1d的回转半径(16.92 Å)与P25(16.81 Å)十分接近, 而与TNTs-2d的回转半径(13.35 Å)差距较大, 据此推断TNTs-1d与P25的介观结构较相近。即, TNTs-1d中包含一部分尚未开始解体的P25结构和少量解体后形成的纳米级碎片, TNTs-2d中P25则接近完全解体, 并开始重组为钛酸纳米管。TNTs-3d的回转半径(15.85 Å)较之TNTs-2d又有所上升, 且与TNTs-4d接近, 表明两者钛酸纳米管含量进一步增加。
2.3 比表面积与孔径分布分析TNTs-1d, TNTs-2d, TNTs-3d和TNTs-4d这4种阶段产物以及二氧化钛(P25)的比表面积、孔径分布和孔体积等由N2吸附/脱附等温线获得。各种材料的比表面积等性能数据如表 3所示。
| 样品名称 | 比表面积/ (m2·g-1) |
孔体积/ (m3·g-1) |
平均孔径/ nm |
最可几孔径/ nm |
| P25 | 51.14 | 0.185 | 14.06 | 2.25 |
| TNTs-1d | 86.66 | 0.178 | 7.99 | 2.08 |
| TNTs-2d | 169.66 | 0.353 | 8.09 | 2.08 |
| TNTs-3d | 138.99 | 0.332 | 9.27 | 2.2 |
| TNTs-4d | 165.8 | 0.332 | 7.78 | 2.23 |
从表 3可以看出, TNTs-2d, TNTs-3d和TNTs-4d的比表面积及孔体积比较接近, 而与TNTs-1d和P25差距较大。P25的比表面积为51.14 m2/g, TNTs-1d较P25有明显的增加, 为86.66 m2/g, 而TNTs-2d, TNTs-3d和TNTs-4d的比表面积均在100 m2/g以上。孔体积方面, P25与TNTs-1d比较接近, 约为0.18 cm/g左右; TNTs-2d, TNTs-3d和TNTs-4d的孔体积为0.33~0.35 cm3/g。P25的平均孔径为14.06 nm, 而TNTs系列样品相比之下, 平均孔径都明显缩小, 为8~9 nm。4种TNTs阶段产物中, TNTs-2d和TNTs-4d的比表面积最大, TNTs-3d的平均孔径最大。
图 3为P25和TNTs系列样品的孔径分布。对比吸附支孔径分布(图 3(b))可以发现, 脱附支(图 3(a)) TNTs系列样品在3~4 nm处有一个孔径分布峰, 是由抗拉强度效应(tensile strength effect, TSE)引起的假峰[18-19]。因此, 对于TNTs系列样品, 吸附支得到的孔径分布更准确。从图 3(b)可知, TNTs系列样品的最可几孔径均在2~2.2 nm范围内。根据国际纯粹与应用化学协会(IUPAC)的定义, 孔径小于2 nm的称为微孔。因此, 所有样品的最可几孔径均已接近微孔范围。同时, TNTs系列样品的最可几孔径均在2~2.2 nm范围内, 且不随水热反应时间的增加而变化。说明在水热反应过程中, [TiO6]八面体这一基本机构并没有遭到破坏, 样品结构的改变只发生在不同[TiO6]八面体的连接方式上。

|
| 图 3. P25与TNTs系列样品的孔径分布 Figure 3. Pore size distribution of various products and P25 |
从表 3还可以发现, P25最可几孔径虽然在2.2 nm左右, 但是其平均孔径显著大于TNTs系列样品, 说明原料P25本身并不具有太多的孔状结构。随着水热反应的开始, 样品内部发生改变, 产生大量直径在20 nm以下的孔状结构, 进而验证了P25样品在水热反应过程中发生结构解体。水热反应48小时的时候孔体积最大, 生成的孔状结构最多, 此时P25解体最彻底。水热反应72小时的时候孔体积略有减小, 这是由于此时生成一种规整有序的结构。当水热反应达到96小时, 孔体积不变, 平均孔径减小, 说明此时孔状结构再次增加, 样品结构再次趋向无序化, 即管状结构开始部分解体。
2.4 Cd (Ⅱ)吸附等温线为深入阐述TNTs系列样品的形貌结构对金属离子吸附行为的影响, 图 4描述TNTs系列样品对Cd (Ⅱ)的吸附等温线。随着平衡浓度的增大, Cd (Ⅱ)的吸附量逐渐增大, 最后趋于平衡。且Cd (Ⅱ)的饱和吸附量大小顺序为TNTs-1d > TNTs-3d > TNTs-4d > TNTs-2d。与多壁碳纳米管(10.86 mg/g)、贝得石(42.01 mg/g)、黄土(9.37 mg/g)和活性炭(19.50 mg/g)相比, 吸附容量高出很多[9]。为了描述TNTs系列样品对Cd (Ⅱ)的吸附等温线, 分别采用Langmuir模型, Freundlich模型, Langmuir-Freundlich模型进行拟合。

|
| 图 4. TNTs系列样品对Cd (Ⅱ)的吸附等温线 Figure 4. Adsorption isotherms of Cd (Ⅱ) onto various TNTs products |
Langmuir吸附模型假设:吸附剂表面均匀; 吸附质之间没有相互作用力; 吸附为单层吸附; 吸附平衡后是动态平衡, 吸附速率与解析速率相同。公式如下:
| $ {Q_{\text{e}}} = \frac{{{Q_{\text{m}}}b{C_{\text{e}}}}}{{1 + b{C_{\text{e}}}}} $ | (6) |
其中, Qe(mg/g)和Ce(mg/L)分别为平衡吸附量和吸附平衡时溶液中Cd (Ⅱ)的浓度, Qm(mg/g)为最大单分子层吸附量, b为与吸附自由能相关的常数。
Freundlich模型为经验模型, 它假设吸附剂表面非均匀且不局限于单层吸附。公式如下:
| $ {Q_{\text{e}}} = {K_{\text{F}}}{C_{\text{e}}}^{1/n} $ | (7) |
式中, KF为与吸附量有关的Freundlich常数(mg/g), n为与吸附剂强度相关的异质性因子。
Langmuir-Freundlich模型为修正模型, 公式如下:
| $ {Q_{\text{e}}} = \frac{{{Q_{\text{m}}}b{C_{\text{e}}}^n}}{{1 + b{C_{\text{e}}}^n}} $ | (8) |
吸附等温式对实验数据的拟合结果如表 4所示。三参数Langmuir-Freundlich模型拟合结果r2 > 0.9, 与实验结果更接近。从TNTs-1d至TNTs-4d, 平衡吸附量分别为189.26, 154.62, 182.50和164.83 mg/g。TNTs-1d与TNTs-3d具有近似相等的平衡吸附容量, 且明显高于TNTs-2d和TNTs-4d。已有研究表明, TNTs表面存在均匀的表面活性位点, 且Cd (Ⅱ)在TNTs表面的吸附为单分子层吸附[14]。本研究结果表明, 吸附到TNTs系列样品上的Cd (Ⅱ)与材料之间可能存在相互作用。
| 实验 | Langmuir模型 | Freundlich模型 | Langmuir-Freundlich模型 | |||||||||
| Qm/(mg·g-1) | b/(L·mg-1) | R2 | KF/(mg·g-1) | n | R2 | Qm/(mg·g-1) | b/(L·mg-1) | n | R2 | |||
| TNTs-1d | 242.14 | 0.04 | 0.8347 | 36.29 | 2.67 | 0.6924 | 189.26 | 0.001 | 2.44 | 0.9466 | ||
| TNTs-2d | 195.51 | 0.05 | 0.8539 | 32.62 | 2.72 | 0.7067 | 154.62 | 0.003 | 2.27 | 0.9548 | ||
| TNTs-3d | 245.52 | 0.04 | 0.8958 | 27.90 | 2.27 | 0.7837 | 182.50 | 0.002 | 2.18 | 0.9745 | ||
| TNTs-4d | 209.61 | 0.05 | 0.8646 | 32.52 | 2.63 | 0.7174 | 164.83 | 0.003 | 2.23 | 0.9604 | ||
从材料表征结果可知, 水热法制备钛酸纳米管的过程经历了二氧化钛源结构解体→钛酸纳米管形成→钛酸纳米管解体的过程。TNTs-3d样品代表其中形成钛酸纳米管这一阶段的样品, 具有最为规整的形貌, 因而其平衡吸附容量最大。
2.5 吸附量与材料孔径的关系表 5列出不同水热反应时间合成的TNTs系列样品的结构参数及对Cd (Ⅱ)的平衡吸附量。吸附时间为Cd (Ⅱ)吸附量达到平衡吸附量95%时所用的时间。TNTs-2d, TNTs-3d和TNTs-4d在结构方面与TNTs-1d有比较大的差别, 因此对吸附的研究主要集中在TNTs-2d, TNTs-3d和TNTs-4d三者的相互对比上。
| 样品 | 平衡吸附量/ (mg·g−1) |
吸附时间/ min |
回转半径/Å | 比表面积/ (m2·g−1) |
孔体积/ (cm3·g−1) |
平均孔径/nm |
| P25 | - | - | 16.81 | 51.14 | 0.185 | 14.06 |
| TNTs-1d | 189.26 | 2.9 | 16.92 | 86.66 | 0.178 | 7.99 |
| TNTs-2d | 154.62 | 4.3 | 13.35 | 169.66 | 0.353 | 8.09 |
| TNTs-3d | 182.50 | 3.0 | 15.85 | 138.99 | 0.332 | 9.27 |
| TNTs-4d | 164.83 | 2.6 | 17.02 | 165.80 | 0.332 | 7.78 |
| 说明:吸附时间为达到平衡吸附量95%时的时间。 | ||||||
从表 5可以看出, TNTs-1d和TNTs-3d对Cd (Ⅱ)的吸附量最高, TNTs-2d与TNTs-4d有显著的差别。随着水热反应时间的延长, TNTs系列样品的回转半径逐渐增加, 吸附平衡时间逐渐缩短, 这与吸附量的变化规律不一致。因此, 样品的回转半径与平衡吸附量无直接关系, 可能与平衡时间有关。
TNTs-2d, TNTs-3d和TNTs-4d的孔体积均在0.33~0.35 cm3/g范围内, 差异较小, 因此, 样品的孔容量也与平衡吸附量无直接关系。相比之下, TNTs-3d的比表面积和平均孔径显著大于TNTs-2d和TNTs-4d, 这可能与样品的吸附容量有关。
3 结论1) 水热时间分别为1, 2, 3, 4天, 合成了4种钛酸纳米管不同形成阶段的系列产物, 粉末XRD表征证实均为单斜晶胞结构。
2) SAXS和N2吸附/脱附表征证实, 水热法制备钛酸纳米管经历了二氧化钛源结构解体→钛酸纳米管形成→管状结构解体的过程, TNTs-3d钛酸纳米管具有最为规整的管状形貌。
3) 吸附等温线结果表明, Langmuir-Freundlich模型能够更好地拟合吸附等温结果, 并且Cd (Ⅱ)的吸附量大小顺序为: TNTs-3d > TNTs-1d > TNTs-4d > TNTs-2d。
4) 样品的回转半径、孔体积对吸附量影响较小, 而比表面积和平均孔径可能会影响吸附容量。
| [1] | Chen Q, Peng L M. Structure and applications of titanate and related nanostructures. International Journal of Nanotechnology, 2007, 4(1/2): 44–63 DOI:10.1504/IJNT.2007.012314 . |
| [2] | Kasuga T, Hiramatsu M, Hoson A, et al. Formation of titanium oxide nanotube. Langmuir, 1998, 14(12): 3160–3163 DOI:10.1021/la9713816 . |
| [3] | Kasuga T, Hiramatsu M, Hoson A, et al. Titania nanotubes prepared by chemical processing. Advan-ced Materials, 1999, 11(15): 1307–1311 DOI:10.1002/(ISSN)1521-4095 . |
| [4] | Chen Q, Zhou W Z, Du G H, et al. Trititanate nanotubes made via a single Alkali treatment. Advanced Materials, 2002, 14(17): 1208–1211 DOI:10.1002/1521-4095(20020903)14:17<1208::AID-ADMA1208>3.0.CO;2-0 . |
| [5] | Wang T, Liu W, Xu N, et al. Adsorption and desorption of Cd (Ⅱ) onto titanate nanotubes and efficient regeneration of tubular structures // 36th International Convention on Information & Communi-cation Technology Electronics & Microelectronics (MIPRO). Opatija, 2013: 379-386 |
| [6] | Yao B D, Chan Y F, Zhang X Y, et al. Formation mechanism of TiO2nanotubes. Applied Physics Letters, 2003, 82(2): 281–283 DOI:10.1063/1.1537518 . |
| [7] | Chen Y C, Lo S L, Kuo J. Pb (Ⅱ) adsorption capacity and behavior of titanate nanotubes made by micro-wave hydrothermal method. Colloids and Surfaces A, 2010, 361: 126–131 DOI:10.1016/j.colsurfa.2010.03.017 . |
| [8] | Du A J, Sun D D, Leckie J O. Sequestration of cadmium ions using titanate nanotube. Journal of Hazardous Materials, 2011, 187: 401–406 DOI:10.1016/j.jhazmat.2011.01.053 . |
| [9] | Xiong L, Chen C, Chen Q, et al. Adsorption of Pb (Ⅱ) and Cd (Ⅱ) from aqueous solutions using titanate nanotubes prepared via hydrothermal method. Journal of Hazardous Materials, 2011, 189(3): 741–748 DOI:10.1016/j.jhazmat.2011.03.006 . |
| [10] | Liu W, Wang T, Alistair G L, et al. Adsorption of Pb2+, Cd2+, Cu2+ and Cr3+ onto titanate nanotubes: competition and effect of inorganic ions. Science of the Total Environment, 2013, 456/457: 171–180 DOI:10.1016/j.scitotenv.2013.03.082 . |
| [11] | Yang D J, Sarina S, Zhu H Y, et al. Capture of radioactive cesium and iodide ions from water by using titanate nanofibers and nanotubes. Angewandte Chemie International Edition, 2011, 50(45): 10594–10598 DOI:10.1002/anie.201103286 . |
| [12] | 盛国栋, 杨世通, 赵东林, 等. 静态法和EXAFS技术研究Eu (Ⅲ)在钛酸纳米管上的吸附行为和微观机制. 中国科学B辑:化学, 2012, 42(1): 60–73. |
| [13] | Suetake J, Nosaka A Y, Hodouchi K, et al. Charac-teristics of titanate nanotube and the states of the confined so dium ions. Journal of Physical Chemistry C, 2008, 112(47): 18474–18482 DOI:10.1021/jp8069223 . |
| [14] | Lin K S, Cheng H W, Chen W R, et al. Synthesis, characterization, and adsorption kinetics of titania nanotubes for basic dye wastewater treatment. Adsor-ption, 2010, 16(1): 47–56 . |
| [15] | Liu J L, Luo M B, Yuan Z Z, et al. Synthesis, characterization, and application of titanate nanotubes for Th (Ⅳ) adsorption. Journal of Radioanalytical and Nuclear Chemistry, 2013, 298(2): 1427–1434 DOI:10.1007/s10967-013-2607-7 . |
| [16] | 张月, 陈清, 龚巍巍, 等. 钛酸钠纳米线的合成和结构. 北京大学学报:自然科学版, 2007, 43(1): 125–131. |
| [17] | 朱育平. 小角X射线散射理论、测试、计算及应用. 北京: 化学出版社, 2008. |
| [18] | Gregg S J, Sing K S W. Adsorption, surface area, and porosity. 2nd ed. London: Academic Press, 1982. |
| [19] | Groen J C, Peffer L A A, Perez-Ramirez J. Pore size determination in modified micro-and mesoporous materials, Pitfalls and limitations in gas adsorption data analysis. Microporous and Mesoporous Materials, 2003, 60: 1–17 DOI:10.1016/S1387-1811(03)00339-1 . |
 2016, Vol. 52
2016, Vol. 52