(a)短腿巢湖龙(标本 GMPKU-P-3086)头骨左侧视; (b)短腿巢湖龙(标本 GMPKU-P-3086)右侧上颌骨及其着生齿及一右侧齿骨齿牙冠; (c)短腿巢湖龙(标本 GMPKU-P-3086)牙根部位的折形牙质; (d)龟山巢湖龙(标本 GMPKU-P-3267)头骨腹视, 绿色区域为上颌, 红色区域为下颌, 灰色区域为牙齿
图1 标本照片及部分结构的CT图像
Fig. 1 Photos and CT images of the studied specimens
北京大学学报(自然科学版) 第60卷 第2期 2024年3月
Acta Scientiarum Naturalium Universitatis Pekinensis, Vol. 60, No. 2 (Mar. 2024)
doi: 10.13209/j.0479-8023.2024.002
国家自然科学基金(40920124002, 41920104001)、高等学校博士学科点专项科研基金(20120001110072)、安徽省自然资源厅科技项目(2021-k-13)和安徽省公益性地质工作项目(2021-g-2-16)资助
收稿日期: 2023–04–04;
修回日期: 2023–04–25
摘要 对产自安徽省巢湖市马家山剖面下三叠统奥伦尼克阶斯帕斯亚阶南陵湖组上段的短腿巢湖龙标本(GMPKU-P-3086)进行研究, 根据 CT 扫描数据重建牙齿及前颌骨、上颌骨和齿骨的三维模型。通过对模型进行观察和度量, 并与实际标本进行对比, 发现以下短腿巢湖龙牙齿新的特征: 1)颌骨上存在连续的牙槽沟, 且内具浅的牙槽窝, 牙齿为亚槽生齿; 2)牙齿的大小和形状呈周期性变化, 显示奇偶相间的交替模式; 3)口腔前部发育单牙列, 替换齿位于功能齿的远中位置; 4)口腔后部发育双牙列, 替换齿列位于功能齿的舌侧–远中位置。短腿巢湖龙的牙齿特征与早三叠世基干鱼龙类短尾鱼龙和歌津鱼龙具有一致性, 可能代表鱼龙类牙齿的原始特征, 并反映捕压式食性群团地理分布的广泛性。
关键词 短腿巢湖龙; 早三叠世; 牙齿替换; CT 扫描
牙齿替换现象在非哺乳类脊椎动物中普遍存在。牙齿的替换速率和替换模式取决于代谢成本与生长、磨损补偿和饮食适应等功能需求之间的平衡[1–2], 具有重要的生态意义。因此, 牙齿的发育和替换模式在各种现生和化石类群的研究中受到关注[3–7]。然而, 由于鱼龙类(ichthyosauroforms)标本保存的牙齿世代数量通常较少, 目前对其牙齿替换的了解十分有限。关于鱼龙牙齿替换最早的研究是Von Zittel[8]对单颗鱼龙牙齿替换过程的简要描述。其后, Edmund[9]基于鱼龙属某未定种的吻部碎片连续切片, 描述了其牙齿的替换模式。Motani[10]基于当时的研究成果, 简要地总结了已知鱼龙的牙齿替换模式。之后, Maxwell 等[11]从谱系演化的角度, 进一步完善了前者的总结。迄今为止, 早三叠世鱼龙的牙齿替换信息仅从短尾鱼龙(Grippia longirostris)和歌津鱼龙(Utatsusaurus hataii)等少数几个物种的有限标本中获知[10]。其中, 在短尾鱼龙和柔腕短吻龙等一些鱼龙物种中发现多齿列现象。在一些植食性和杂食性的爬行动物类群(如二叠纪的 captorhi-nid)中, 多齿列的保留被认为与牙齿的替换过程相关[12], 但该特征在鱼龙类中的发育机制尚不明确。
发现于早三叠世奥伦尼克期斯帕斯亚期的巢湖龙(Chaohusaurus)是目前已知层位最低、特征最原始的鱼龙之一, 是当时海洋生态系统中的重要捕食者[13]。研究巢湖龙的牙齿替换信息, 能够为研究鱼龙类的起源与早期演化历史提供新的证据。近年来, CT 扫描和三维复原重建技术因能无损地获取化石内部精细结构信息而备受瞩目, 已将其应用于一般观察方法不易揭示的牙齿特征研究中, 为多角度观察、精细测量与定量化分析提供了新的方法。
本研究使用高分辨率 CT 扫描和 3D 重建技术, 研究短腿巢湖龙副模标本 GMPKU-P-3086 的牙齿特征及着生方式, 通过牙齿结构确定每颗牙齿的发育阶段, 测量每颗牙齿的大小与形状信息, 并推断牙列的模式和牙齿替换的方式, 同时与短腿巢湖龙标本 GMPKU-P-3093、龟山巢湖龙标本 GMPKU-P-3267 以及巢县巢湖龙标本 GMPKU-P-3188 进行比较, 探究其形态特征的异同。
本文的研究材料(标本号为 GMPKU-P-3086)(图1(a))为短腿巢湖龙的副模标本, 保存于北京大学地质博物馆(Geological Museum of Peking University, GMPKU)。标本发掘自安徽省巢湖马家山剖面下三叠统奥伦尼克阶斯帕斯亚阶南陵湖组上段第 633 层灰色中厚层泥灰岩中。据 δ13Ccarb 记录推算天文旋回, 确定该层的地质年龄为约 248.43Ma[14]。据其四肢长度较短的特征, 推断标本为一雌性个体, 头骨保存长度为 83.63mm, 除吻尖部分缺失外, 基本上完整立体保存。头骨受背腹向压扁和轻微侧向压扁, 略向右侧倾斜变形, 后部关节脱落。研究材料GMPKU-P-3267(图 1(b))为龟山巢湖龙标本, 头骨呈腹视保存。
研究区位于安徽省巢湖市马家山剖面, 距巢湖东北岸约 2km。巢湖地区位于扬子板块东北缘, 郯庐断裂东侧, 华北板块与扬子板块的缝合带, 特提斯构造与太平洋构造交汇处, 中生代以来构造活动强烈, 以印支运动形成的 NNE-SSW 向褶皱构造为主, 伴随发育一系列断层[15]。
研究区古地理位置为下扬子海盆边缘的深水陆棚[16], 出露较完整且连续的二叠纪–三叠纪海相地层, 生物化石丰富。下三叠统主要由薄层泥岩与灰岩韵律性互层组成, 并呈现明显的多级岩性旋回序列[17], 产出菊石、双壳类、鱼类和鱼龙化石, 反映陆棚至浅海台地沉积为主的沉积环境。中三叠统仅出露蒸发台地相的东马鞍山组。中三叠世后, 本区全面抬升为陆地, 三叠纪晚期受印支运动 NW-SE向挤压影响而发生显著的褶皱造山运动[18]。下三叠统南陵湖组地层位于平顶山向斜的核部, 地层序列由北向南总体上呈现由老到新的变化趋势。碳酸盐岩沉积微相研究指示该段地层呈现向上变浅序列, 由下部的外缓坡脚–深海盆地边缘环境向上渐变为外缓坡的沉积环境[19]。马家山剖面出露南陵湖组中段顶部至上段, 底部主要为瘤状灰岩, 中上部主要为泥岩与泥灰岩互层。巢湖龙动物群化石集中产自南陵湖组上段的底部, 岩性主要为灰色薄层灰岩与泥灰岩互层, 位于 Neospathodus triangularis牙形石带及 Subcolombites 菊石带内[20], 时代为早三叠世奥伦尼克期斯帕斯亚期。
本研究基于 CT 扫描图像, 对标本 GMPKU-P-3086 进行三维重建。显微 CT 扫描在中国地质大学(北京)进行, 扫描电子束能量为 165kV, 扫描电流为 52μΑ, 分辨率为 34μm。使用可视化三维图像处理软件 VG Studio MAX 2.2 进行三维重建, 通过逐层确定牙齿结构的范围, 还原标本牙齿的三维形态。随后, 使用该软件的度量工具测定牙冠高度和宽度。使用研究级体视显微镜 Nikon SMZ25 对标本GMPKU-P-3267 进行观察与测量。

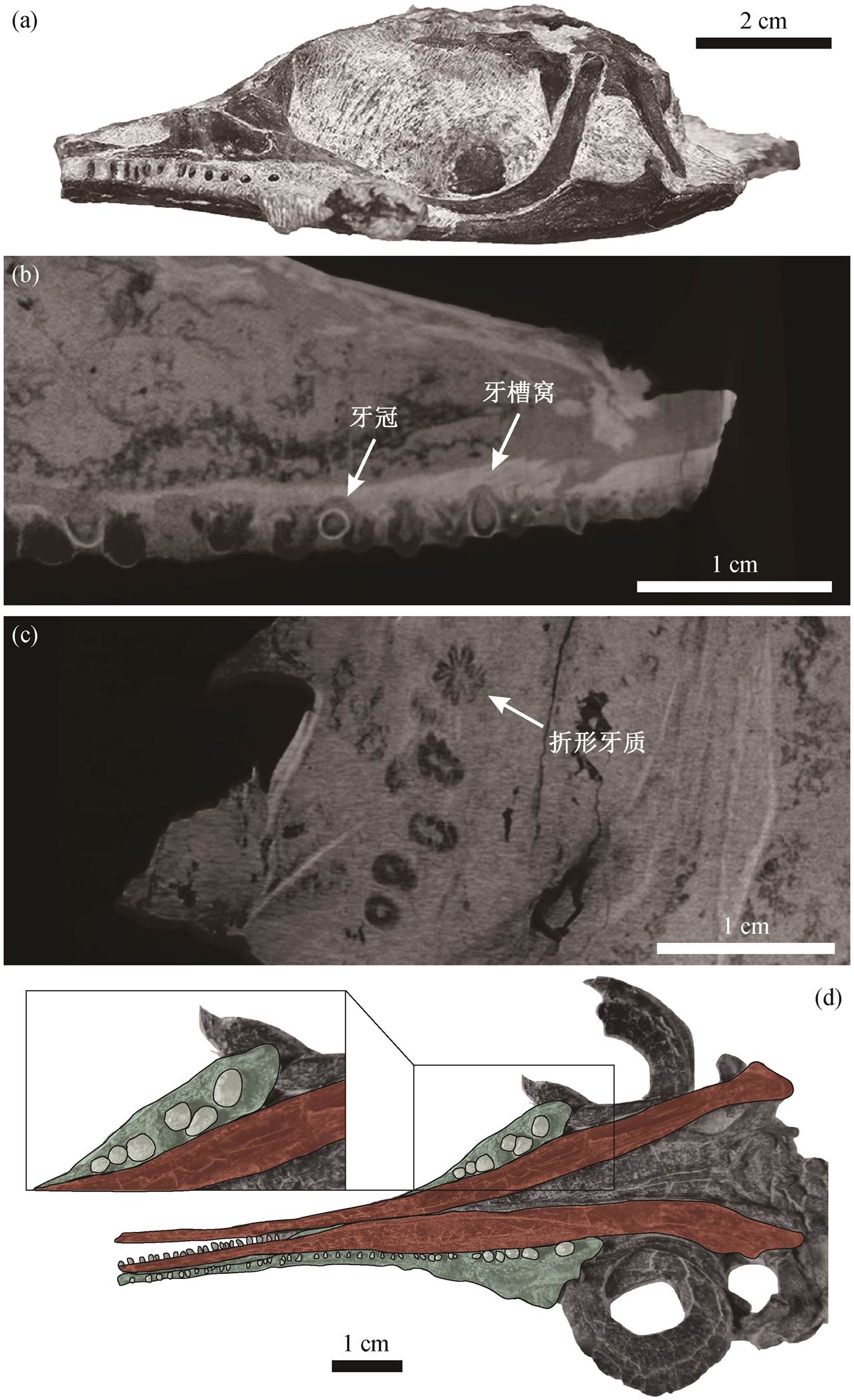
(a)短腿巢湖龙(标本 GMPKU-P-3086)头骨左侧视; (b)短腿巢湖龙(标本 GMPKU-P-3086)右侧上颌骨及其着生齿及一右侧齿骨齿牙冠; (c)短腿巢湖龙(标本 GMPKU-P-3086)牙根部位的折形牙质; (d)龟山巢湖龙(标本 GMPKU-P-3267)头骨腹视, 绿色区域为上颌, 红色区域为下颌, 灰色区域为牙齿
图1 标本照片及部分结构的CT图像
Fig. 1 Photos and CT images of the studied specimens
在标本 GMPKU-P-3086 的 CT 图像中, 于前颌骨、上颌骨和齿骨上发现牙齿, 共计 92 颗。在 Mo-tani[21]的描述中, 巢湖龙的齿冠较宽, 即前后方向上的长度小于唇侧–舌侧方向上的长度。CT 图像显示, 牙冠横切面呈近圆形, 未观察到明显的定向压扁现象(图 1(b))。牙冠顶部圆润, 牙釉质从牙顶部向牙根方向逐渐减薄, 直至消失, 牙釉质层消失处为牙冠与牙根的分界。牙冠表面具有间距较宽、不甚明显的纵向纹饰, 牙冠表面较光滑。相比于牙冠, 牙根突然膨大, 牙本质层剧烈折叠, 形成折形牙质(plicidentine)(图 1(c))。牙根最大横向宽度约为牙冠最大横向宽度的 2 倍。牙齿着生在牙槽窝中(图 1 (b)), 牙槽窝较浅, 窝内容纳部分牙根, 有部分牙根暴露在牙槽窝外部, 可能生前被软组织包裹。牙根底部与着生骨骼紧密接触, 推断牙根底部与牙槽窝长合。上颌骨齿列在眼眶后缘之前的区域发育。
在短腿巢湖龙中识别出以下 4 类牙齿。
1)功能齿: 牙冠和牙根完整, 高度相对较大, 位于牙槽窝中, 直立生长。
2)替换齿: 仅见牙冠。在爬行动物中, 牙本质基质与牙釉质基质首先在牙尖部形成, 随后从牙冠向牙根方向矿化[1,11], 因此推断这些仅有牙冠的牙齿是尚处于发育阶段的替换齿。
3)残余的牙根: 仅见牙根部分。有些位于牙槽窝内, 有些与骨骼无接触, 可能为被替换的功能齿脱落折断后残留下来的部分牙根。
4)脱落的功能齿: 仅见牙冠而未见牙根, 或牙根保存不全, 牙冠大小与完整的功能齿牙冠相当, 靠近空的牙槽窝上方。此外, 还发现牙冠碎片, 位于左侧上颌骨第 16 颗与第 17 颗牙齿之间舌侧位置, 此处没有对应的空牙槽窝, 可能该处牙槽窝已经被新的牙齿占据。牙齿重建模型如图 2(a)所示。
将以上所有类型归纳编号, 统计结果如下。
前颌骨齿: 两侧前颌骨前端缺失; 保存的部分, 其左右侧各有 4 个牙位。左侧第 1 牙位为空的牙槽窝。左侧第 3 牙位及右侧第 1 牙位上为替换齿, 尚未与前颌骨接触, 相应位置存在牙槽窝(图 2(d))。
上颌骨齿: 上颌骨保存完整。左侧上颌骨共计有 17 个牙位, 前段为单牙列, 第 10 牙位及之后为双牙列。第 11 牙位上为残余牙根, 位于第 10 牙位功能齿的唇侧, 可能与第 10 牙位功能齿处于同一牙槽窝内。第 16 和 17 牙位的功能齿间舌侧位置存在一枚牙冠碎片。第 15 牙位上为替换齿, 位于舌侧牙列。第 5 牙位上为左侧上颌最大牙齿, 位于该颌象限中部偏后位置。右侧上颌骨共计有 19 个牙位, 前端为单牙列, 第 11 牙位及之后为双牙列, 与左侧上颌骨齿左右对称。第 11 和 17 牙位处为空的牙槽窝, 第 12 牙位处为脱落的功能齿, 与上颌骨无接触, 向舌侧倾斜, 位于第 11 牙位上的空的牙槽窝上方, 可能是从第 11 牙位脱落的。第 14 牙位处由于只存在牙冠, 且位于后部区域的唇侧牙列, 可能也是相应位置脱落的功能齿。第 1, 4 和 8 牙位处为替换齿, 其中第 1 和 4 牙位处的替换齿极其微小。第 4 牙位于第 3 牙位处功能齿底部, 上颌骨内部, 被骨骼包围。第 12 牙位处为右侧上颌最大牙齿, 位于该颌象限后部(图 2(d))。
齿骨齿: 两侧齿骨前端缺失。左侧齿骨保留 30个牙位, 前段为单牙列, 从第 13 牙位处开始变为双牙列(图 2(e))。第 1, 22 和 30 牙位处为残余的牙根, 第 19 牙位处为空的牙槽窝, 后部双牙列区的空牙槽窝和残余牙根均位于唇侧, 残余牙根均不与齿骨直接接触。唇侧牙列的第 26 牙位处功能齿牙根保存不全, 与牙槽窝接触较少, 可能已经开始脱落。第7, 15 和 20 牙位处为替换齿, 均位于舌侧, 其中第 20牙位处替换齿位于第 19 牙位处空牙槽窝舌侧, 应具有对应的替换关系。第 25 牙位处为左侧下颌最大牙齿, 位于该颌象限后部。右侧齿骨保留 31 个牙位, 前段为单牙列, 从第15牙位处开始变为双牙列, 空间上与左侧发生转变的位置左右对称, 但下颌相比于上颌发生转变的空间位置更靠前端(图 2(f))。第 1, 9, 18 和 25 牙位处为残余牙根, 构成 7~9 个牙位近似的等间隔分布, 后部的残余牙根位于唇侧牙列。第 4 牙位处为一折断的功能齿, 下部牙根不全, 呈半月形, 弯向其舌侧。第 29 牙位处功能齿顶部有牙冠碎片。第 5 牙位处替换齿位于第 4 牙位处折断的功能齿舌侧底部。第 23 牙位处替换齿位于舌侧牙列, 牙冠已发育至功能齿大小。第 30 牙位处替换齿位于舌侧牙列。第 31 牙位处为右侧下颌最大牙齿, 位于该颌象限最后部。
测量的特征数据包括牙冠的高度和宽度。由于牙冠横切面均为近圆形, 对每颗牙齿而言, 牙冠横截面不存在长宽的差异。根据获得的数据, 计算得出牙冠形态指数和牙齿相对大小参数。
牙冠形态参数的定义为牙冠高度与牙冠最大横截面长、短轴长度之平均值的比值[21], 由于此处牙冠呈近圆形, 不存在明显的长轴与短轴之分, 因此将牙冠形态参数简化为牙冠的高度与宽度的比值。牙齿相对大小参数为最大一颗牙齿的牙冠高度与头骨宽度的比值, 这里为了反映每颗牙齿的大小信息, 计算了每颗牙齿的相对大小。关于头骨宽度的定义, Massare[22]提出以下 3 个标准: 1)两侧方骨间的距离; 2)两侧下颌关节间的距离; 3)上颞孔前缘平台处最大头骨的宽度。Motani[10]认为鱼龙类颅骨顶部的标志是沿上颞孔前存在一个大的平台, 其前缘呈抛物线状, 在头骨顶部呈弧形。Mazin[23]认为平台的最前端是下颌内收假性颞内肌的附着点。因此, 该处与口的张合及牙齿的功能有重要联系, 可以将该处头骨宽度视为计算所需的头骨宽度。在此, 与Motani[10]对短尾鱼龙牙齿的研究进行对照后, 采用第一种标准。由于标本左侧变形较严重, 本文采用右侧宽度的两倍作为头骨宽度, 采用电子数显卡尺进行测量, 精度为 0.01mm。
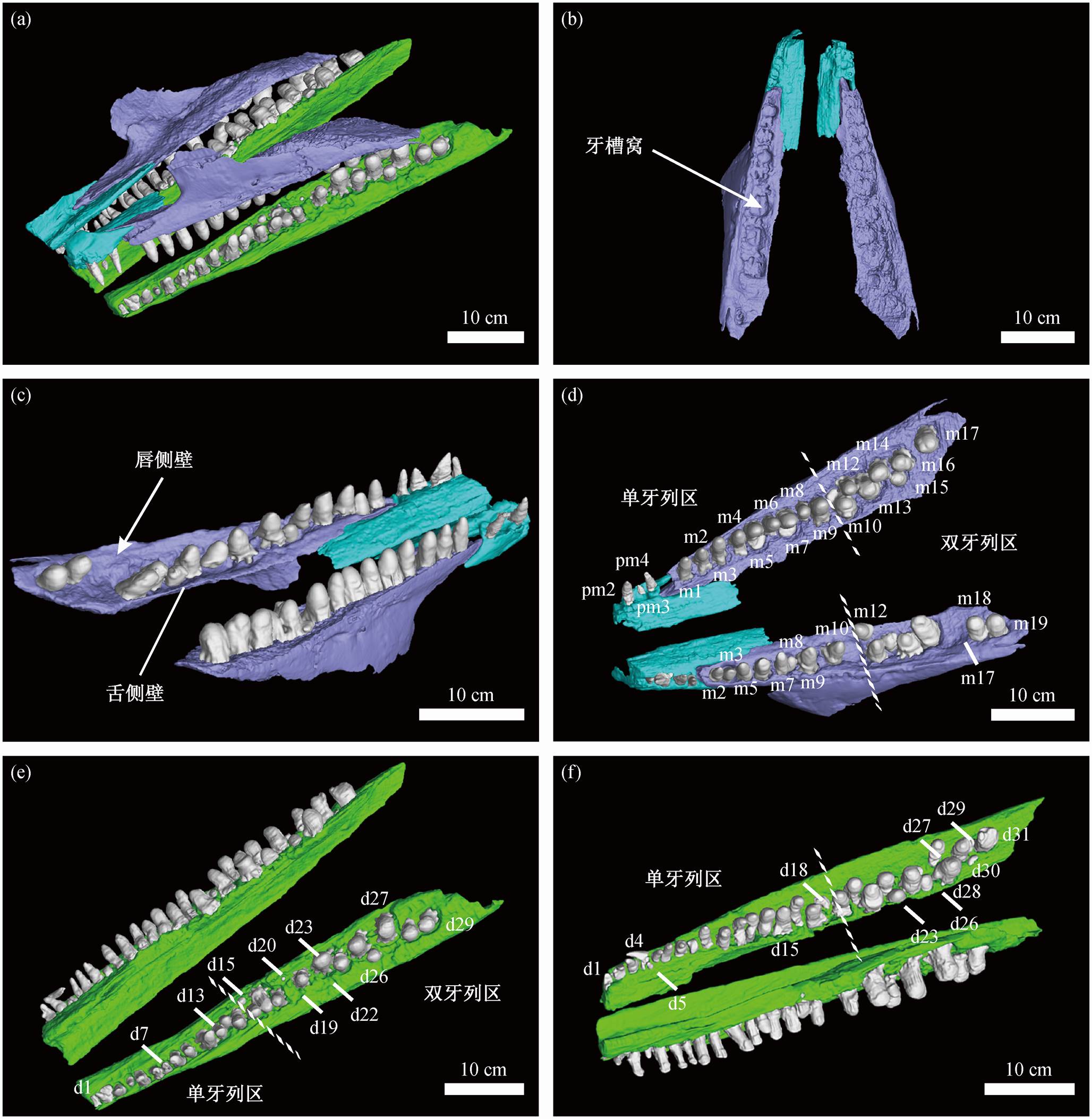
(a)头骨前部结构; (b)前颌骨及上颌骨的牙槽窝, 腹视; (c)前颌骨及上颌骨的牙槽沟; (d)上颌牙列结构, 腹视; (e)和(f)下颌牙列结构, 背视。蓝色为前颌骨, 紫色为上颌骨, 绿色为齿骨, 灰白色为牙齿。pm: 前颌骨; m: 上颌骨; d: 齿骨
图2 短腿巢湖龙GMPKU-P-3086牙齿三维重建结果
Fig. 2 3D reconstructed model of the teeth of Chaohusaurus brevifemoralis GMPKU-P-3086
标本 GMPKU-P-3086 每一颌象限的牙齿形态及大小分布如图 3 所示。可以看出, 牙齿相对大小与形态参数存在奇偶相间的变化趋势, 相邻两颗较大的牙齿间总是存在一颗相对较小的牙齿。在更大的尺度上, 存在周期性的变化, 右侧下颌表现尤为明显, 一个周期约为 7~9 颗牙齿。就总体趋势而言, 除左侧上颌未表现出明显的变化外, 功能齿的大小从前到后逐渐增大。从前到后, 形态参数从超过 1.5 逐渐递减至小于 1.0, 反映牙齿形态从前部较为细长的特征向后部较为钝圆的特征过渡式转变。
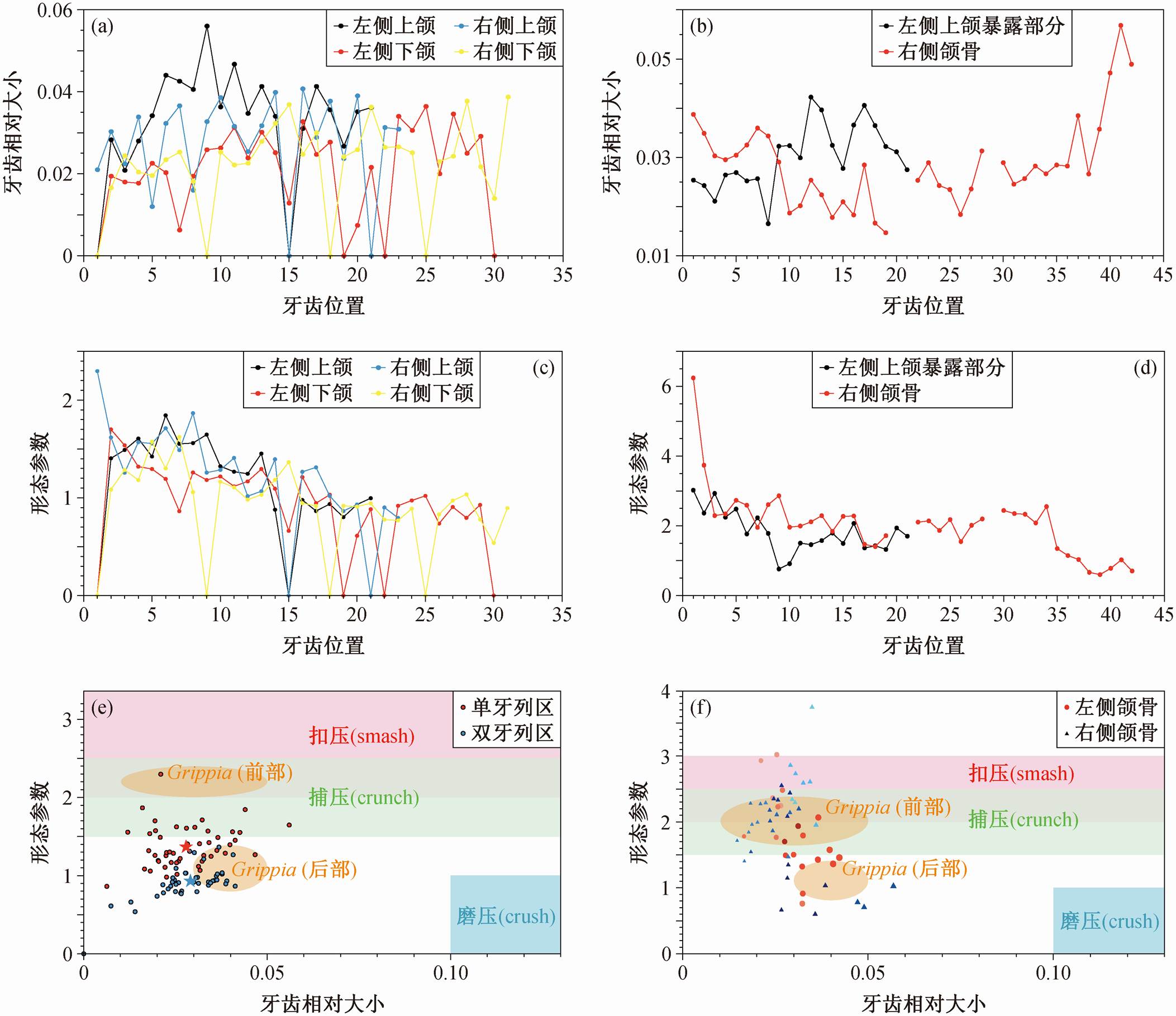
(a)和(b)牙齿相对大小沿颌骨的分布; (c)和(d)牙冠形态参数沿颌骨的分布; (e)和(f)功能齿捕食功能投图, 其中五角星为相应区域牙齿参数的平均值对应位置。(f)中符号的大小代表牙齿的相对大小; 符号的颜色越深, 代表牙齿的位置越靠后
图3 短腿巢湖龙GMPKU-P-3086 ((a), (c)和(e))与龟山巢湖龙GMPKU-P-3267 ((b), (d)和(f))牙齿测量数据
Fig. 3 Measurements of teeth in Chaohusaurus brevifemoralis GMPKU P-3086 ((a), (c) and (e)) and Chaohusaurus geishanensis GMPKU-P-3267 ((b), (d) and (f))
在标本 GMPKU-P-3086 中, 牙齿着生的骨骼存在连续的牙槽沟, 且牙槽沟唇侧壁高于舌侧壁; 存在浅的独立牙槽窝(图 2(b)), 基于牙齿与牙槽窝底部骨骼直接接触, 推测牙齿底部与牙槽窝长合; 牙根形态膨大, 发育折形牙质(图 1(c))。折形牙质的存在是鱼龙类的共有衍征[24]。Motani[10]曾经基于Romer[25]和 Edmund[9]的研究, 归纳出羊膜动物的5 种牙齿着生方式, 即槽生齿、长合槽生齿、亚槽生齿、侧生齿和端生齿。在鱼龙中, 主要存在 4 种牙齿着生方式, 即亚槽生齿、长合槽生齿、鱼龙型槽生齿和沟槽生齿(aulacodont)。着生方式的分类主要依据 5 个特征, 即牙槽沟的有无、牙槽窝及其深度、牙齿与牙槽的长合关系以及牙根形状即牙槽沟唇侧壁与舌侧壁的相对厚度[10]。亚槽生齿类型要求存在具有浅牙槽窝的牙槽沟, 牙齿底部与牙槽窝长合, 牙根膨大且弯折, 牙槽沟唇侧壁高于舌侧壁。依据上述分类标准可以判断, 短腿巢湖龙属于亚槽生齿类型。
在标本 GMPKU-P-3086 中, 上颌骨齿与齿骨齿在前部形成单牙列, 在后部形成双牙列。在双牙列区, 舌侧牙列的每颗牙齿都位于相邻两颗唇侧牙列牙齿中线的舌侧。在上颌中, 单牙列约在第 10~11牙位转变为双牙列; 在下颌中, 单牙列大致在第13~15 牙位转变为双牙列。单牙列区的长度与双牙列区的长度近似相等。在转变点位置, 左右两侧对称, 但是相比于上颌, 下颌转变点位置略微靠近吻端。两牙列中的功能齿均位于牙槽窝中。在龟山巢湖龙 GMPKU-P-3276 中, 左侧上颌骨后端出露的牙齿也呈现双牙列的排列模式(图 1(d))。
中生代鱼龙牙齿的着生方式, 早三叠世以亚槽生齿为主导, 中三叠世同时存在亚槽生齿、长合槽生齿和鱼龙型槽生齿, 晚三叠世则主要为沟槽生齿类型[26]。迄今为止, 早三叠世鱼龙中仅有歌津鱼龙和短尾鱼龙牙齿着生方式的研究信息。仙台歌津鱼龙前部为侧生齿, 后部为亚槽生齿[21]; 短尾鱼龙后部为亚槽生齿[10]。亚槽生齿见于许多早期四足动物类群中, 如油页岩蜥[27]、一些大鼻龙类[28–29]以及一些爬行形类。由于许多基干羊膜动物的牙齿均着生于牙槽之中, Bertin 等[30]认为亚槽生齿或槽生齿可能是羊膜动物牙齿着生方式的祖征。短腿巢湖龙的亚槽生特征进一步支持 Motani[10]对鱼龙类牙齿着生方式演化趋势的总结, 然而, 牙齿着生方式在羊膜类演化历程中变化显著, 因而其系统发生学意义相对有限[30]。
边缘齿多牙列现象在硬骨鱼与软骨鱼类群中较为常见, 但在羊膜动物中较少发现。在现生蜥蜴中, 美洲鬣蜥科角蜥亚科是具有多牙列的唯一类群, 且这一现象被解释为发育异常的结果[31]。在化石类群中, 石炭–二叠纪早期的四足动物大鼻龙类(Cap-torhinus)中, 部分类群具有多牙列现象, 如 Captorhi-nusaguti 在口腔前部为单牙列, 口腔后部则为双牙列[32]。大鼻龙类是爬行类中最早分化出去的一支, 代表着爬行动物的原始特征。在鱼龙类中, 目前仅有部分类群被报道存在多牙列现象, 包括早三叠世的短尾鱼龙(Grippia longirostris)[10]、Gulosaurus he-lmi[33]、龟山巢湖龙(Chaohusaurus geishanensis)[34]和柔腕短吻龙(Cartorhynchus lenticarpus)[35], 中三叠世的卡塔克新民龙(Xinminosaurus catactes)[36]、弗拉斯异齿鱼龙(Phalarodon fraasi)[37]、Mixosaurus nordenskioeldii[38]、Tholodus schmidi[38]和 Ompha-losaurus nevadanus。然而, 关于多牙列形成机制与功能的讨论仍然较少。
舌侧牙列可被解释为功能齿或替换齿。在现生爬行动物中, 前颌骨、上颌骨和齿骨均只发育单牙列, 但多期替换齿可以同时存在。现生非哺乳类脊椎动物终生替换牙齿, 即使是过去曾经被认为不替换牙齿的具有端生齿的爬行动物, 也被观察到非常缓慢地替换牙齿[39]。随着比较解剖学和分子生物学的发展, 关于羊膜动物牙齿替换的发育机制已经成为共识, 即在羊膜动物每一颌象限内, 功能齿舌侧各存在一个决定牙齿发育的牙板(dental lamina), 替换齿在其中发育, 并向唇侧移动, 最终替换先前发育的功能齿。在具有齿系(dental batteries)的类群中, 舌侧牙列是因替换过程的停止而形成的。对于鱼龙类, Motani[26]认为在短尾鱼龙中, 舌侧牙列是替换齿, 而唇侧牙列为功能齿。卡塔克新民龙的双牙列也被认为是由一列功能齿和一列替换齿构成[36]。在标本 GMPKU-P-3086 中, 牙齿形态和大小存在奇偶交替与周期性变化的趋势(图 3(a)和(c)), 可由此区分出至少两期牙齿, 处于不同发育阶段。
根据牙齿替换的“抑制区”理论(zone of inhibition theory)[40], 每颗牙蕾由抑制区包围, 抑制区内不能发育新的牙齿; 抑制区的半径随时间减小, 至相邻两抑制区不再重叠, 新的牙齿在两抑制区的间隙中发育。在标本 GMPKU-P-3086 中, 牙齿形态与大小的周期性可能是牙齿替换时抑制过程的结果。此外, 标本 GMPKU-P-3086 中所有未成熟的替换齿均发现于舌侧牙列, 而残余牙根均分布于唇侧牙列。一般而言, 在爬行动物中, 临近成熟功能齿的最近一组替换齿略大于功能齿[41]。在标本 GMPKU-P-3086中, 舌侧牙列的功能齿平均牙冠高度为 2.17mm, 略微大于唇侧牙列功能齿平均高度 2.11mm, 类似现象亦见于其他具有多牙列的鱼龙类中(如柔腕短吻龙)。据此可以推断, 虽然在发育意义上短腿巢湖龙的舌侧牙列仍为替换齿(即每一功能齿伴随不多于一颗替换齿), 但在功能上可能已经开始承担参与捕压食物的作用(图 3(c)和(f))。
Tucker 等[42]认为, 替换齿列的数目可能与替换速率相关。在现生爬行动物中, 鳄类的替换齿列数目较少, 牙齿一年一换; 有鳞类存在 3~4 列替换齿, 牙齿每年替换 4 次。标本 GMPKU-P-3086 中只有一列替换齿列, 可能与其较低的替换速率相关。
在有关鱼龙类系统发育分析的研究中, 多数研究支持其为基干的鳞龙型类[43–44], 少数研究认为其为基干的初龙型类[45]。现生初龙型类成员鳄类的牙齿着生方式为槽生齿, 替换齿与其对应功能齿在同一牙槽中发育。现生有鳞类的牙齿着生方式为侧生齿, 按照替换齿的移动方向, 可以区分出以下 3种牙齿替换模式: 1)巨蜥型(varanid mode), 替换齿位于功能齿远中位置, 替换不引起吸收孔出现, 功能齿的脱落是由着生骨的吸收导致; 2)美洲鬣蜥型(iguanid mode), 替换齿位于功能齿舌侧位置, 通过吸收孔移入功能齿牙髓腔内部, 至脱落时, 功能齿仅残余尖端部分; 3)中间类型, 即前两种模式的过渡类型, 存在于蛇蜥类中, 替换齿位于功能齿舌侧远中位置, 向唇侧近中方向移动, 并通过吸收孔取代功能齿[1]。
标本 GMPKU-P-3086 中, 在口腔前部的单牙列区, 替换齿位于功能齿的远中位置; 亦存在一颗替换齿位于功能齿底部的现象, 与功能齿处于同一牙槽窝内, 并吸收其部分牙根; 在后部的双牙列区, 舌侧牙列的替换齿位于相应功能齿的远中端舌侧, 与有鳞类的中间型替换模式相符。在其他早三叠世鱼龙类中, 歌津鱼龙和短尾鱼龙的替换齿均发育于牙槽窝外部, 位于功能齿的远中端舌侧, 向近中–唇侧方向移动, 并替换功能齿[10], 亦与有鳞类的中间型替换模式相符。
在本次研究的两件标本中, 均存在牙齿形态从前到后由细长转变为钝圆的现象, 这一特征在许多具有多牙列的鱼龙类中亦有发现, 如短尾鱼龙[10]、Gulosaurus helmi[33]和 Phalarodon fraasi[37]。参照Massare[22]的分类标准, 短腿巢湖龙 GMPKU-P-3086的前部牙齿与捕压功能相关, 可能用于捕食具有硬壳的食物类型。南陵湖组上段产出的巢湖龙与菊石、双壳类、节肢类和鱼类等伴生, 它们当中可能有巢湖龙捕食的对象。在吻部保存完整的巢县巢湖龙标本 GMPKU-P-3188 中, 吻部前缘至最后一颗牙齿出露位置的长度为 5.755cm; 另一件短腿巢湖龙标本 GMPKU-P-3093 中, 吻部前缘至最后一颗牙齿出露位置的长度为 3.500cm。根据个体大小推测, 巢湖龙动物群中的原哥伦布菊石、王氏克氏蛤、海浪蛤、复杂弱海扇、正海扇、圆形拟克氏蛤和巢湖安琪虾可能是巢湖龙的捕食对象。口腔后部咬合力最大, 多齿列的保留增加了牙齿间的接触面积, 可能增加了适应硬质食物的捕食方式的功能优势。早三叠世具多牙列的歌津鱼龙和短尾鱼龙的牙齿形态亦指向捕压型捕食方式, 说明多牙列可能与食用硬质食物的捕食方式具有功能上的普遍联系。上述早三叠世鱼龙类分布于东特提斯洋和西特提斯洋, 反映出捕压式食性具有广泛的地理分布。
本文通过 CT 扫描与三维重建技术技术, 揭示早三叠世短腿巢湖龙(标本 GMPKU-P-3086)的牙齿新信息, 增进了对该物种发育过程与生态功能的了解, 得到以下结论。
1)短腿巢湖龙前颌骨齿、上颌骨齿和齿骨齿的大小和形态存在奇偶交替及周期性变化规律, 指示存在一组功能齿和一组替换齿。
2)短腿巢湖龙前颌骨齿和齿骨齿在前部形成单牙列, 在后部形成双牙列, 分别对应不同的牙齿替换模式。多牙列现象为早期鱼龙类的衍生特征。
3)短腿巢湖龙牙齿着生方式为亚槽生齿, 符合早期鱼龙类的衍生特征, 与早三叠世鱼龙歌津鱼龙和短尾鱼龙一致。
4)短腿巢湖龙的牙齿形态指示捕压式捕食方式, 亦与歌津鱼龙和短尾鱼龙一致。
短腿巢湖龙的牙齿特征反映出基干鱼龙类牙齿在形态、着生方式、替换模式及生态功能上的相似性, 可能代表鱼龙类牙齿的原始特征, 并反映出捕压式食性群团在地理分布上的广泛性。
致谢 北京大学地球与空间科学学院胡田芬技师帮助修理标本, 沈阳师范大学殷亚磊博士在软件使用方面进行指导, 北京大学地球与空间科学学院孙作玉副教授、柴珺博士和博士研究生李家春在论文写作过程中提出建设性意见, 在此一并致谢。
参考文献
[1] Berkovitz B K B, Shellis R P. The teeth of non-mammalian vertebrates. London: Academic Press, 2017
[2] Osborn J W. Tooth replacement: efficiency, patterns and evolution. Evolution, 1975, 29(1): 180–186
[3] He Y, Makovicky P J, Xu X, et al. High-resolution computed tomographic analysis of tooth replacement pattern of the basal neoceratopsian Liaoceratops yan-zigouensis informs ceratopsian dental evolution. Sci-entific Reports, 2018, 8(1): 5870
[4] Zahradnicek O, Horacek I, Tucker A S. Tooth develo-pment in a model reptile: functional and null gene-ration teeth in the gecko Paroedura picta. Journal of Anatomy, 2012, 221(3): 195–208
[5] Fastnacht M. Tooth replacement pattern of Colobor-hynchus robustus (Pterosauria) from the Lower Creta-ceous of Brazil. Journal of Morphology, 2008, 269 (3): 332–348
[6] Schwarz D, Kosch J C D, Fritsch G, et al. Dentition and tooth replacement of Dicraeosaurus hansemanni (Dinosauria, Sauropoda, Diplodocoidea) from the Ten-daguru Formation of Tanzania. Journal of Vertebrate Paleontology, 2015, 35(6): e1008134
[7] Snyder A J, LeBlanc A R H, Jun C, et al. Thecodont tooth attachment and replacement in bolosaurid parare-ptiles. PeerJ, 2020, 8: e9168
[8] Von Zittel K A. Handbuch der palaeontologie: Vol. 5. München: Oldenbourg, 1890
[9] Edmund A. Tooth replacement phenomena in the lower vertebrates. Toronto: The University of Toronto Press, 1960
[10] Motani R. Redescription of the dentition of Grippia longirostris (Ichthyosauria) with a comparison with Utatsusaurus hataii. Journal of Vertebrate Paleonto-logya, 1997, 17(1): 39–44
[11] Maxwell E E, Caldwell M W, Lamoureux D O. Tooth histology, attachment, and replacement in the Ichthy-opterygia reviewed in an evolutionary context. Paläon-tologische Zeitschrift, 2011, 86(1): 1–14
[12] Olroyd S L, LeBlanc A R H, Araújo R, et al. Histology and μCT reveal the unique evolution and development of multiple tooth rows in the synapsid Endothiodon. Scientific Reports, 2021, 11(1): 16875
[13] Zhou M, Jiang D Y, Motani R, et al. The cranial osteology revealed by three-dimensionally preserved skulls of the Early Triassic ichthyosauriform Chao-husaurus chaoxianensis (Reptilia: Ichthyosauromor-pha) from Anhui, China. Journal of Vertebrate Paleon-tology, 2017, 37(4): doi: 10.1080/02724634.2017.1343 831
[14] Fu W, Jiang D Y, Montaez I P, et al. Eccentricity and obliquity paced carbon cycling in the Early Triassic and implications for post-extinction ecosystem reco-very. Scientific Reports, 2016, 6: 27793
[15] 于鹏, 宋传中. 巢湖地区构造应力场研究及动力分析. 合肥学院学报(综合版), 2010, 20(2): 78–81
[16] 左景勋, 童金南, 邱海鸥, 等. 巢湖地区早三叠世碳氧同位素地层对比及其古生态环境意义. 地球与环境, 2003, 31(3): 26–33
[17] 童金南, 赵来时, 左景勋, 等. 安徽巢湖地区下三叠统综合层序. 地球科学: 中国地质大学学报, 2005, 30(1): 40–46
[18] 刘柯, 宋立军, 刘学锋. 巢湖北部褶皱构造变形特征及其构造物理模拟. 安徽地质, 2022, 32(1): 12–14
[19] 张钰莹, 江大勇, 付宛璐, 等. 安徽巢湖下三叠统含巢湖龙动物群地层微相特征及古环境. 古地理学报, 2014, 16(5): 761–768
[20] Tong J, Yin H. The Lower Triassic of South China. Journal of Asian Earth Sciences, 2002, 20(7): 803–815
[21] Motani R. Redescription of the dental features of an Early Triassic ichthyosaur, Utatsusaurus hataii. Journal of Vertebrate Paleontology, 1996, 16(3): 396–402
[22] Massare J A. Tooth morphology and prey preference of Mesozoic marine reptiles. Journal of Vertebrate Paleontology, 1987, 7(2): 121–137
[23] Mazin J M. Grippia longirostris Wiman, 1929, un Ichthyopterygia primitif du Trias inférieur du Spits-berg. Bulletin du Muséum National d`Histoire Nature-lle, Section C, 1981, 3(4): 317–340
[24] Cuthbertson R S, Russell A P, Anderson J S. Rein-terpretation of the cranial morphology of Utatsusau- rus hataii (Ichthyopterygia) (Osawa Formation, Lower Triassic, Miyagi, Japan) and its systematic implica-tions. Journal of Vertebrate Paleontology, 2013, 33(4): 817–830
[25] Romer A S. The early evolution of land vertebrates. Proceedings of the American Philosophical Society, 1956, 100(3): 157–167
[26] Motani R. Temporal and spatial distribution of tooth implantations in Ichthyosaurs // Motani R. Ancient marine reptiles. San Diego: Academic Press, 1997: 81–103
[27] Reisz R R. A diapsid reptile from the Pennsylvanian of Kansas. Lawrence: Natural History Museum, Univer-sity of Kansas, 1981
[28] Reisz R R, Liu J, Li J L, et al. A new captorhi- nid reptile, Gansurhinus qingtoushanensis, gen. et sp. nov., from the Permian of China. Naturwissenschaften, 2011, 98(5): 435–441
[29] Liebrecht T, Fortuny J, Galobart À, et al. A large, multiple-tooth-rowed captorhinid reptile (Amniota: Eureptilia) from the Upper Permian of Mallorca (Ba-learic Islands, Western Mediterranean). Journal of Vertebrate Paleontology, 2017, 37(1): e1251936
[30] Bertin T J C, Thivichon-Prince B, LeBlanc A R H, et al. Current perspectives on tooth implantation, attach-ment, and replacement in Amniota. Frontiers in Phy-siology, 2018, 9: 1630
[31] Scarpetta S G, Bell C J. Novel and bizarre abnor-malities of the tooth row in Side-Blotched Lizards (Uta) and Rock Lizards (Petrosaurus). The Anatomical Record, 2020, 303: 2014–2025
[32] Leblanc A, Reisz R R. Patterns of tooth development and replacement in captorhinid reptiles: a comparative approach for understanding the origin of multiple tooth rows. Journal of Vertebrate Paleontology, 2015, 35(3): e919928
[33] Cuthbertson R S, Russell A P, Anderson J S. Cranial morphology and relationships of a new grippidian (Ichthyopterygia) from the Vega-Phroso Siltstone Me-mber (Lower Triassic) of British Columbia, Canada. Journal of Vertebrate Paleontology, 2013, 33(4): 831–847
[34] Motani R, You H. Taxonomy and limb ontogeny of Chaohusaurus geishanensis (Ichthyosauria), with a note on the allometric equation. Journal of Vertebrate Paleontology, 1998, 18(3): 533–540
[35] Huang J D, Motani R, Jiang D Y, et al. Repeated evolution of durophagy during ichthyosaur radiation after mass extinction indicated by hidden dentition. Scientific reports, 2020, 10(1): 1–10
[36] Jiang D, Motani R, Hao W, et al. New primitive ichthyosaurian (Reptilia, Diapsida) from the Middle Triassic of Panxian, Guizhou, southwestern China and its position in the Triassic biotic recovery. Progress in Natural Science, 2008, 18(10): 1315–1319
[37] Merriam J C. The skull and dentition of a primitive ichthyosaurian from the Middle Triassic. University of California Publications, Bulletin of the Department of Geology, 1910, 5: 381–390
[38] McGowan C, Motani R. Handbook of paleoherpetolo-gy, part 8 ichthyopterygia. Munich: Verlag Dr. Friedri-ch Pfeil, 2003
[39] Jenkins K M, Jones M E H, Zikmund T, et al. A review of tooth implantation among rhynchocephalians (Lepi-dosauria). Journal of Herpetology, 2017, 51(3): 300–306
[40] Osborn J W. The ontogeny of tooth succession in Lacerta vivipara Jacquin (1787). Proceedings of the Royal Society B: Biological Sciences, 1971, 179: 261–289
[41] Westergaard B, Ferguson M W J. Development of the dentition in Alligator mississippiensis. Early embryo-nic development in the lower jaw. Journal of Zoology, 1986, 210(4): 575–597
[42] Tucker A S, Fraser G J. Evolution and developmental diversity of tooth regeneration. Seminars in Cell and Developmental Biology, 2014, 25/26: 71–80
[43] Motani R, Minoura N, Ando T. Ichthyosaurian rela-tionships illuminated by new primitive skeletons from Japan. Nature, 1998, 393: 255–257
[44] Massare J A, Callaway J M. The affinities and ecology of Triassic ichthyosaurs. Geological Society of Ameri-ca Bulletin, 1990, 102(4): 409–416
[45] Müller J. The relationships among diapsid reptiles and the influence of taxon selection // Arratia G, Wilson V H, Cloutier R. Recent advances in the origin and early radiation of vertebrates. Munich: Verlag Dr. Friedrich Pfeil, 2004: 379–408
Study of the Tooth Replacement of Chaohusaurus brevifemoralis from the Lower Triassic of Chaohu, Anhui Province
Abstract A specimen of Chaohusaurus brevifemoralis (GMPKU-P-3086) from the Lower Triassic in Chaohu City, Anhui Province is examined by using high-resolution CT scan data to create a 3D reconstruction. The reconstructed models include models of teeth, premaxilla, maxilla, and dentary. Through observation and measurement of the model, and comparison with the specimen, the following new features of this basal ichthyosauriformes were found. 1) the implantation is subthecodont based on the presence of a dental groove with shallow sockets at the bottom. 2) the sizes and shapes of the teeth vary periodically and appear as an odd-even alternate pattern. 3) the anterior teeth form a single row, with the replacement tooth setting on the distal position of the functional tooth. 4) Two rows of teeth at the distal parts of the dentary and maxilla are firstly found in Chaohusaurus. The lingual row comprises replacement teeth for the labial row, and each replacement tooth lies disto-lingual of its predecessor. These dental features found in Chaohusaurus brevifemoralis are consistent to that of the Early Triassic ichthyosauriformes,such as Grippia and Utatsusaurus, which might represent a primitive condition of the dental character of ichthyosauri-formes and reflect a broad geographical distribution of crunch feeding guild.
Key words Chaohusaurus brevifemoralis; Early Triassic; tooth replacement; CT scanning