垃圾渗滤液(landfill leachate)是在垃圾填埋过程中因雨水径流和厌氧降解等综合因素产生的高浓度有机废水[1], 其氨氮含量高, 有机污染物种类繁多, 不仅含有简单的烷烃、烯烃、酚类和酯类, 而且含有复杂的卤代烃、酰胺类、多环芳烃和杂环芳烃等化合物[2]。未经处理或处理不当的垃圾渗滤液,一旦进入河流、农田和地下水等自然生态系统, 将严重污染生态环境, 对水生生物造成慢性和积累性的毒性, 对人类健康造成潜在威胁[3–5]。
目前, 垃圾渗滤液的处理方法分为物理方法、化学方法和生物方法。其中, 基于活性污泥的生物处理法具有运行成本低、处理效果好和无二次污染等优点, 广泛应用于垃圾渗滤液处理中。活性污泥中含有丰富的微生物菌群, 可以利用垃圾渗滤液中的污染物作为生长基质, 诱导酶进行同化, 以便维持生物量, 从而实现污染物的转化分解, 达到净化污水的目的[6]。因此, 深入了解活性污泥中微生物的种群结构和功能基因, 对调控污泥微生物组成和提高污水处理效率有重要意义。
近年来, 高通量测序技术迅速发展, 为分析污泥微生物群落组成和动态变化、鉴定功能微生物菌群和功能基因以及研究微生物之间的相互作用关系提供了有力的手段[7]。高通量测序技术已应用于不同废水处理系统微生物的研究中, 如 Zhang 等[8]利用宏基因组测序技术研究 4 个污水处理厂的微生物群落结构, 发现处理生活污水的活性污泥微生物菌群比工业污水具有更高的多样性; Fang 等[9]探究农药废水处理厂活性污泥的优势菌属, 发现区别于工业废水和市政污水活性污泥的细菌属; Joshi 等[10]对焦化废水生物处理系统进行研究, 结果表明 Burkholderiales, Actinomycetales, Rhizobiales, Pseudomonadales 和 Hydrogenophiliales 是重要的功能微生物类群, 芳香双加氧酶、硝化酶和硫氰酸水解酶基因是含氮和含硫污染物生物转化的重要功能基因。不同处理厂的原水特性使其活性污泥呈现独特的细菌群落组成, 从而表现出不同的功能。
目前, 将活性污泥微生物应用于垃圾渗滤液处理体系的研究还比较少。本研究提取垃圾渗滤液处理厂活性污泥的 DNA, 采用 16S rRNA 基因和宏基因组高通量测序手段, 分析污泥中微生物的菌群结构, 解析氮代谢和有机污染物代谢相关的功能基因,探究垃圾渗滤液和其他类型废水处理系统微生物功能基因的差异, 旨在系统地探讨垃圾渗滤液活性污泥的菌群多样性和功能特征, 为构建高效污水生物处理体系奠定理论基础。
1 材料和方法
1.1 样品采集
活性污泥样品采自深圳市罗湖区下坪垃圾填埋场 A/O 生化处理系统中的回流污泥, 采集时间为2019 年 12 月中旬。采样当月该厂生化进水 COD 浓度为 4650 mg/L, NH4+-N 浓度为 1366 mg/L; 生化出水 COD 浓度为 1200 mg/L, NH4+-N 浓度为 11 mg/L。
新鲜的活性污泥样品采集后立即置于冰桶中,运至实验室并于当天处理。样品在 10000 rpm 条件下离心 15 分钟, 去掉上清液, 保留活性污泥用于DNA 提取。
1.2 DNA 提取和高通量测序
采用 PowerSoilTM 试剂盒(MoBio Laboratories Inc., Carlsbad, 美国)提取活性污泥细菌基因组DNA, 使用 Nano Drop 2000 分光光度计(Thermo Fisher Scientific, Waltham, MA, USA)检测提取 DNA的质量和浓度, 使用通用引物 515F(3'-GTGYCAG CMGCCGCGGTAA-5')和 806R(5'-GGACTACNVGG GTWTCTAAT-3')扩增细菌 16S rRNA 基因的 V4区。PCR 产物用 TaKaRa MiNiBEST DNA 片段纯化试剂盒 Ver.4.0 (TaKaRa, 日本)纯化, 然后用凝胶电泳进行质量检查。将基因组 DNA 和 16S rRNA 基因送至诺禾致源(天津)公司, 在 Illumina Hiseq 2500平台上对宏基因组 DNA 和 16S rRNA V4 区进行高通量测序, 分别获得 34.2G 的宏基因组数据和 240M的 16S rRNA 基因数据。
1.3 16S rRNA 基因数据分析
使用 FastQC (v0.11.8)[11]和 Trimmomatic[12]软件查看原始测序数据的质量并进行过滤, 去除低质量的序列。使用 QIIME2[13]软件分析过滤后的 16S rRNA 基因序列。设置 97%的相似性阈值, 对序列进行聚类, 形成可操作分类单元(operational taxonomic units, OTU), 使用 SILVA 非冗余数据库[14]对OTU 进行分类学注释。
1.4 宏基因组数据分析
1.4.1 DNA 组装与分箱(Binning)
使用 FastQC 和 Trimmomatic 软件对宏基因组原始数据进行质量优化后, 采用 metaSPAdes (v3.13.1)[15]组装软件对宏基因组数据进行组装, kmer 值设置为 21, 33, 55, 77, 99 和 127。
宏基因组分箱(Binning)是将宏基因组测序得到的混合了不同生物的序列或序列组装得到的重叠群(contigs)按物种分开归类。本研究首先使用 Bowtie2(v2.2.6)[16]软件, 将质控后的原始数据映射(mapping)到组装得到的 contigs 上, 计算每个 contig 的覆盖率(Coverage), 使用 MaxBin2 (v2.2.7)[17]、MetaBAT(v2.12.1)[18]以及 CONCOCT (v0.4.2)[19]这 3 种不同的Binning 工具提取基因组, 并对基因组去冗余和质量优化。
1.4.2 基因组质量评估和物种注释
使用 CheckM (v1.1.2)软件[20]评估基因组的大小、contig 数量、N50 值、GC 含量、完整度和污染度。计算基因组的质量得分(完整度 − 5 × 污染度)[21],挑选质量得分高于 50 的基因组进行后续分析。使用 GTDB-tk (v1.0.2)软件[22], 对基因组进行分类注释。
1.4.3 基因功能注释
使用 Prodigal 软件[23], 对组装文件和基因组文件进行开放性阅读框(open reading frames, ORFs)预测, 将 ORFs 提交至京都基因百科全书 KEGG (https://www.genome.jp/kegg/pathway.html), 使用 BLAST程序[24], 将 ORFs 与 KEGG 数据库进行比对, 构建基因组的代谢通路图。
2 结果与讨论
2.1 垃圾渗滤液处理厂活性污泥种群结构
活性污泥对污水的处理性能与微生物的种群结构密不可分。对垃圾渗滤液处理厂活性污泥中的微生物进行 16S rRNA 基因测序, 经质量控制后得到440000 条有效序列。经 QIIME2 处理后得到 1258条差异 OTU, 与 SILVA 数据库比对后得到活性污泥微生物的分类学注释结果。
在垃圾渗滤液处理系统活性污泥中共检测到 32 个门(图 1), 其中 Calditrichaeota 是最丰富的门,占样品的 58.77%; 其次是 Proteobacteria (变形菌门)和 Bacteroidetes (拟杆菌门), 分别占样品的 16.80%和 6.19%。这 3 个门的微生物丰度占样品的 80%以上, 其他丰度超过 1%的门还有 Choroflexi (绿弯菌门, 4.29%), Planctomycetes (浮霉菌门, 3.76%), Patescibacteria (髌骨菌门) (1.96%), Acidobacteria (酸杆菌门, 1.52%), Verrucomicrobia (疣微菌门, 1.05%)。

图1 微生物门水平种群结构
Fig. 1 Microbial community composition at phylum levels
在活性污泥中共检测到 334 个属(图 2), 作为Calditrichaeota 门中唯一一个属, Calorithrix 在污泥中占 58.77%, 说明相对于其他属, Calorithrix 属更容易在高 BOD、高 COD 和高 NH4+-N 的垃圾渗滤液处理体系中生存并富集。作为典型的氨氧化细菌,亚硝化单胞菌属 Nitrosomonas 占体系的 1.30%, 是体系中丰度第二的属, 其余属水平的物种丰度均未超过 1%。在体系中还存在大量未分类到属的物种,说明垃圾渗滤液处理厂活性污泥中可能存在现有数据库中未收录的新属。
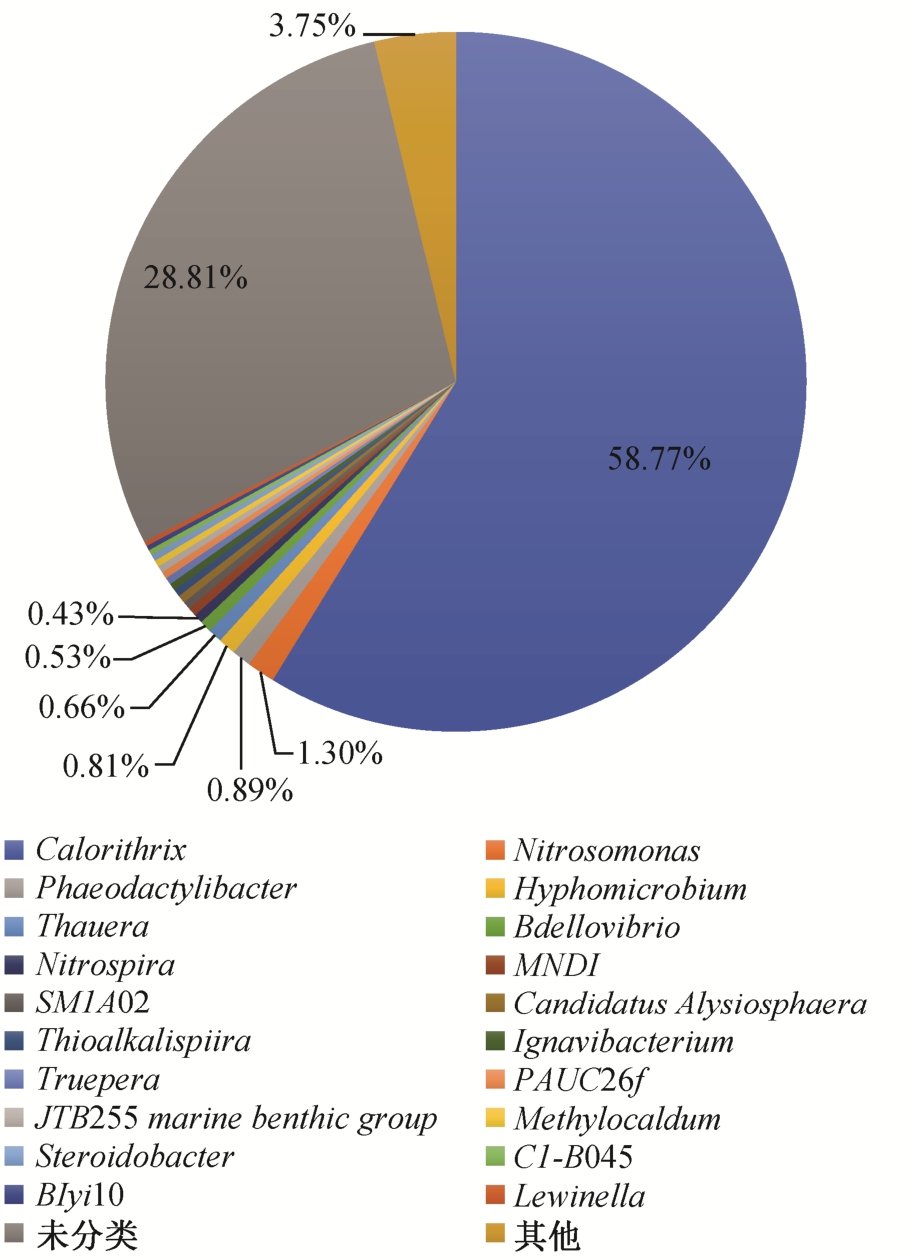
图2 微生物属水平种群结构
Fig. 2 Microbial community composition at genus levels
Proteobacteria, Bacteroidetes 和 Choroflexi 是污水处理系统中常见的微生物(表 1), 在不同类型的污水处理厂和活性污泥工艺中都被报道为优势菌门[8–9], 在本研究的样品中也具有较高的丰度, 说明垃圾渗滤液与其他污水处理系统活性污泥的种群结构具有一定的相似性。Proteobacteria 在污水处理系统中最为常见, 丰度可达 78.86%, 多项研究证明 Proteobacteria 可降解多种有机污染物, 并可减轻污染物引起的生物毒性[25–28]。Bacteroidetes 参与聚合物和复杂有机物质的降解, 可以将包含多糖和蛋白质的死细胞分解为简单的有机分子(例如乙醇和乳酸),这些简单的分子可以被其他物种代谢[29–30]。Chloroflexi 可以合成胞外多糖, 对污泥团聚体的形成起着重要作用, 并可通过丝状网络增强生物膜的结构[31–33]。也有研究表明 Acidobacteria, Firmicutes 和Actinobacteria 在营养去除过程中起着重要作用, 是废水处理系统中广泛存在的门[8,34]。
表1 不同污水处理体系活性污泥的优势菌门
Table 1 Dominant phylum of activated sludge in different wastewater treatment systems
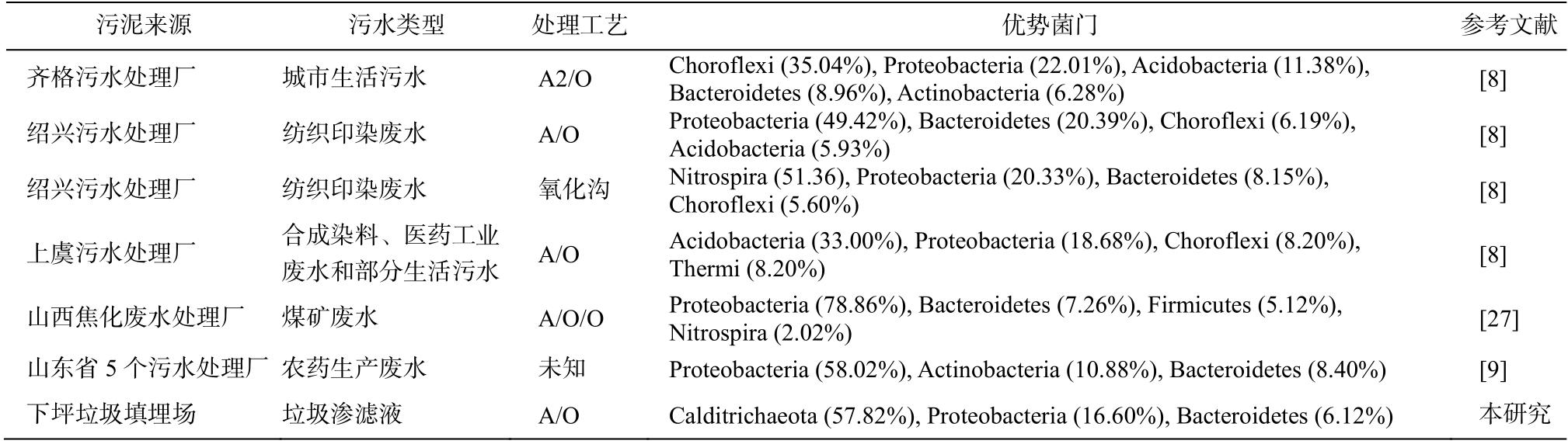
污泥来源 污水类型 处理工艺 优势菌门 参考文献齐格污水处理厂 城市生活污水 A2/O Choroflexi (35.04%), Proteobacteria (22.01%), Acidobacteria (11.38%),Bacteroidetes (8.96%), Actinobacteria (6.28%) [8]绍兴污水处理厂 纺织印染废水 A/O Proteobacteria (49.42%), Bacteroidetes (20.39%), Choroflexi (6.19%),Acidobacteria (5.93%) [8]绍兴污水处理厂 纺织印染废水 氧化沟 Nitrospira (51.36), Proteobacteria (20.33%), Bacteroidetes (8.15%),Choroflexi (5.60%) [8]上虞污水处理厂 合成染料、医药工业废水和部分生活污水 A/O Acidobacteria (33.00%), Proteobacteria (18.68%), Choroflexi (8.20%), Thermi (8.20%) [8]山西焦化废水处理厂 煤矿废水 A/O/O Proteobacteria (78.86%), Bacteroidetes (7.26%), Firmicutes (5.12%),Nitrospira (2.02%) [27]山东省5 个污水处理厂 农药生产废水 未知 Proteobacteria (58.02%), Actinobacteria (10.88%), Bacteroidetes (8.40%) [9]下坪垃圾填埋场 垃圾渗滤液 A/O Calditrichaeota (57.82%), Proteobacteria (16.60%), Bacteroidetes (6.12%) 本研究
然而, 作为本研究样品中最优势的门, Calditrichaeota 门却未在污水处理系统的相关研究中报道过。Calditrichaeota 是一个新发现的细菌门, 分为Caldithrix 属和 Calorithrix 属, 其中 Caldithrix 属首次在从爱琴海浅水热液沉积物获得的 16S rRNA 克隆文库中发现[35], 从大西洋中脊深海热液喷口样品中首次分离出来[36], Calorithrix 属则是在 2016 年从俄罗斯Kunashir 岛的海底热液喷口中首次发现并分离[37]。Marshall 等[38]分析海洋沉积物的 16S rRNA基因数据集, 结果表明 Calditrichaeota 以高丰度分布于全球海底, 占细菌群落的 6.7%。目前发现的Calditrichaeota 微生物均为化能异养菌, 具有降解蛋白质基质的能力, 能够利用丙酮酸、淀粉、纤维二糖和木糖聚糖等多种能量底物[35–39]。垃圾渗滤液是一种高浓度的有机废水, 富含可生物降解的挥发性脂肪酸(VFA)以及难降解的腐殖质(腐殖酸、富里酸), COD 和 BOD 浓度可达数千至几万[40–41], 大量的有机污染物可能是 Calditrichaeota 丰度高的原因。
目前报道的 Calditrichaeota 均来自海洋沉积物,本研究首次发现污水处理系统中 Calditrichaeota 门微生物的存在, 并且具有较高的丰度, 扩大了对Calditrichaeota 门的认知, 表明 Calditrichaeota 具有更大的生理生态位。
2.2 垃圾渗滤液处理系统活性污泥功能注释
2.2.1 总体水平功能注释
对垃圾渗滤液处理厂活性污泥中的微生物进行宏基因组测序, 组装后获得 739205 条 contigs, 通过 ORF 预测得到 1012950 条 ORFs, 与 KEGG 数据库比对, 进行功能注释, 如图 3 所示。结果表明,垃圾渗滤液处理系统活性污泥微生物在碳水化合物代谢(Carbohydrate metabolism)、氨基酸代谢(Amino acid metabolism)、能量代谢(Energy metabolism)和辅酶和维生素代谢(Cofactor and vitamin biosynthesis)中的基因丰度最高, 分别占注释基因的 17.36%,12.77%, 8.14%和 4.88%, 这些基因与细胞新陈代谢相关, 是微生物赖以生存和生长的基础, 因而丰度最高。活性污泥中还发现与外源有机化合物降解(Xenobiotics of other secondary metabolites)相关的基因, 说明活性污泥在降解有机污染物方面具有一定的潜力。与遗传信息处理相关的基因在体系中也具有较高的丰度, 如复制和修复(Replication and repair)基因占注释基因的 5.01%, 翻译(translation)相关基因占 2.74%, 折叠、分类和降解(Folding,sorting and degradation)基因占2.25%。此外, 体系中还发现信号转导(Signal transduction)、膜传输(Membrane transport)等环境信息处理相关的基因,分别占注释基因的 4.64%和 3.24%, 说明活性污泥微生物之间存在着物质交流和信息传递, 具有一定的相互作用关系。
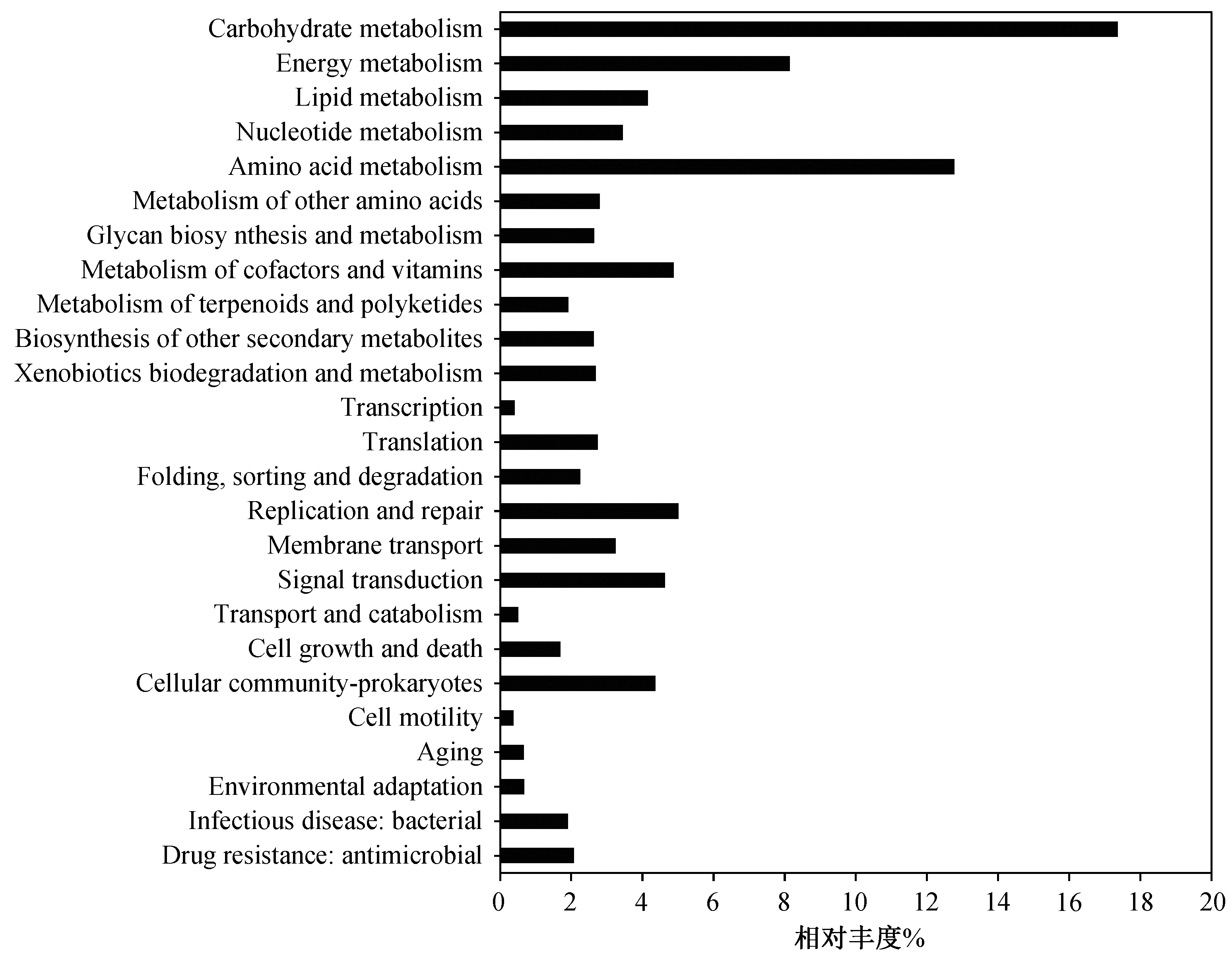
图3 基于KEGG 数据库的功能基因注释
Fig. 3 Function of genes in the activated sludge, annotated by KEGG database
2.2.2 氮循环相关基因功能注释
1) 氮循环相关基因丰度。
脱氮是活性污泥的重要功能之一, 参与氮代谢的功能基因在废水处理中起着至关重要的作用, 因此, 研究氮代谢基因丰度, 构建氮代谢通路是活性污泥微生物研究的一个重要内容。本研究表明, 垃圾渗滤液处理系统活性污泥中存在着 5 种氮代谢途径: 硝化作用、反硝化作用、同化硝酸盐还原、异化硝酸盐还原和氮固定。作为一种直接以氨为电子供体的新型脱氮工艺, 厌氧氨氧化相关基因在体系中没有发现(图 4)。
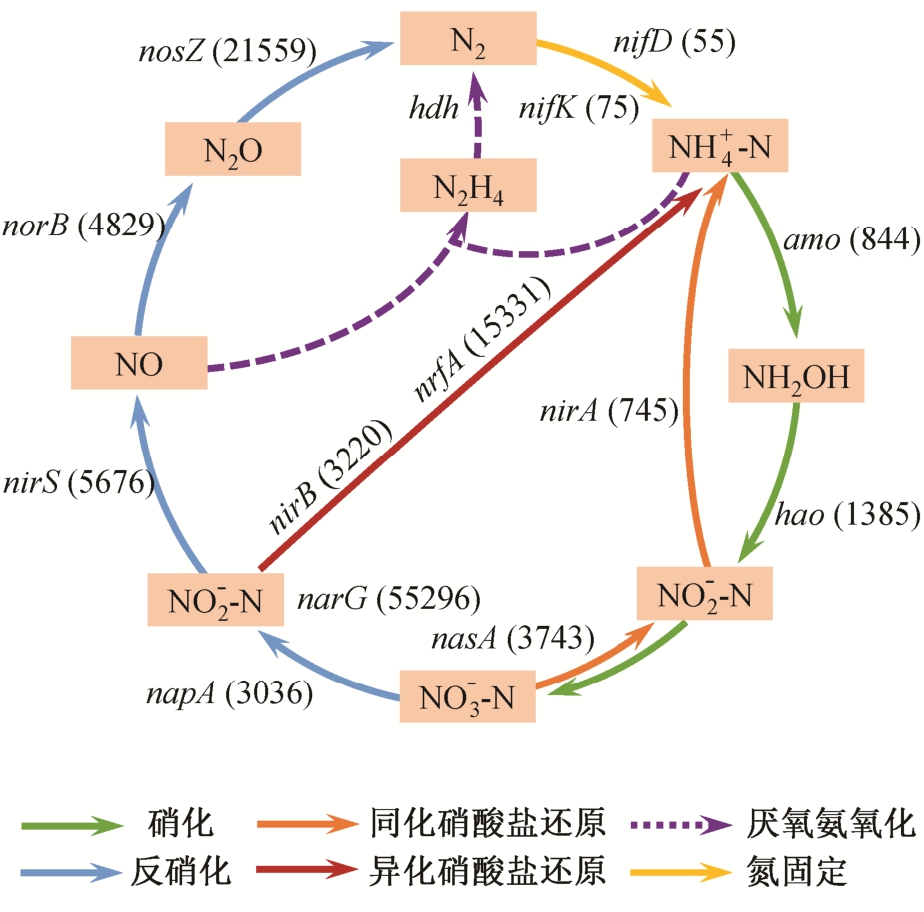
图4 活性污泥氮循环途径及基因丰度
Fig. 4 Nitrogen transformation pathways and gene abundance in the activated sludge
通过计算基因丰度, 我们发现反硝化相关基因在体系中丰度最高, 占 5 个氮循环途径基因总和的78.84%, 其中硝酸盐还原酶 narG 丰度为 55296 hits,远高于其他反硝化基因, 说明部分反硝化作用在硝态氮还原为亚硝态氮的过程中发挥关键作用[42]; 亚硝酸盐还原酶 nirK 和 nirS 的丰度分别为 4254 hits 和5676 hits, 一氧化氮还原酶 norB 的丰度为 4829 hits,一氧化二氮还原酶的功能基因 nosZ 丰度也较高, 共有 21559 条 reads 被注释为该基因。前人研究表明,绝大多数反硝化菌为兼性菌, 代谢途径丰富多样,对 pH 不是特别敏感, 只要环境条件适宜, 反硝化过程就能顺利进行, 这可能是反硝化基因在活性污泥中丰度较高的原因[43]。另一方面, 反硝化作用是将水体中的氮转化为气态氮, 从而从水体中去除的过程, 是脱氮过程的关键途径, 体系中丰富的反硝化功能基因表明垃圾渗滤液活性污泥良好的脱氮性能。
硝化作用相关功能基因在体系中丰度不高, 如催化铵态氮转化为羟胺的氨单加氧酶功能基因 amo丰度为 844 hits, 而催化羟胺转化为亚硝酸盐的羟胺氧化还原酶功能基因 hao 丰度为 1385 hits。Yu 等[44]利用宏基因组和宏转录组的方法研究市政污水处理厂活性污泥的氮循环基因, 结果表明, 尽管活性污泥中硝化功能基因丰度不高, 但这些基因表现出较强的表达活性, 远远高于反硝化等其他氮循环功能基因。
除硝化作用和反硝化作用外, 体系中还发现同化硝酸盐还原和异化硝酸盐还原途径, 即氨化作用。同化硝酸盐还原是硝酸盐被还原成亚硝酸盐和氨,氨被同化成氨基酸, 合成细胞生长所需要的物质,这个过程由 nasA (3743 hits)和 nirA (745 hits)催化完成。异化硝酸盐还原是在在无氧或微氧条件下, 微生物进行的硝酸盐呼吸, 即以 NO3−或 NO2−代替O2 作为电子受体进行呼吸代谢, 这一过程由 nirB(3220 hits)或 nrfA (15331 hits)催化。体系中存在大量的氨化基因, 仅次于反硝化相关基因, 与前人的研究结果[45–46]一致。
2) 氮循环基因分布。
经基因组 Binning 后共获得 158 个基因组, 利用CheckM 对基因组的完整度和污染度进行评估, 共有62 个高质量基因组(完整度 − 5 × 污染度 > 50%)用于后续分析, 基因组的详细信息请访问 http://xbna.pku.edu.cn (以下简称xbna)查看附录 1。
将 Binning 抽取的基因组进行物种注释, 并与 KEGG 数据库比对, 探究体系中氮循环基因在物种上的分布。结果表明, 氨单加氧酶 amo 基因仅存在于 Proteobacteria 门下的 Nitrosomonas, 说明 Nitrosomonas 是活性污泥中起主要作用的氨氧化细菌(AOB)。Wang 等[42]和彭永臻等[46]的研究表明, Nitrosomonas 菌属是一种在活性污泥处理工艺及各类反应器中最常见的 AOB, 能够将进水中氨氮氧化为亚硝态氮。例如, Wang 等[42]采用同步部分硝化–厌氧氨氧化–反硝化生物反应器处理垃圾渗滤液, 证明 Nitrosomonas 是其主要的 AOB 菌属, 与厌氧氨氧化菌共同主导总氮的去除。
在 17 个门的基因组中发现全部或部分反硝化相关基因(图 5)。narG 基因分布最广泛, 主要分布在 Calditrichaeota (33333 hits)、Choroflexi (11566 hits)和 Proteobacteria (3560 hits)门。其中, Calditrichaeota 门 (属水平为 Calorithrix)丰度最高, 占总 narG 的60.28%。napA 基因主要分布在 Proteobacteria (1037 hits)、Planctomycetes (844 hits)和 Verrucomi-crobia(266 hits)门。亚硝酸盐还原酶 nirK 基因主要来源于Choroflexi (2835 hits)、Bacteroidetes (272 hits)和 Deinococcus-Thermus (240 hits), 而 nirS 基因主要来源于 Choroflexi (3041 hits)和 Proteobacteria(1063 hits)。一氧化氮还原酶基因 norB 在 Proteo-bacteria 中丰度最高(1227 hits), Zixibacteria (463 hits)和 Verrucomicrobia (379 hits)次之, 而 norC 基因整体丰度不高。氧化亚氮还原酶 nosZ 基因在多个门中均有分布, 其中 Calditrichaeota 丰度最高(17063 hits), 占总 nosZ 基因的 79.14%, 说明 Calditrichae-ota 对活性污泥中氧化亚氮的还原贡献较大。

图5 硝化作用和反硝化作用的功能微生物
Fig. 5 Functional microorganisms in nitrification and denitrification processes
2.2.3 有机污染物降解相关基因功能注释
1) 有机污染物降解基因的丰度及多样性。
研究表明, 活性污泥不仅可以去除污水中的有机营养物(有机碳、氮和磷等), 对难降解有机污染物的去除也发挥重要的作用[47]。因此, 研究活性污泥中难降解有机污染物的降解基因和功能微生物,对解析污染物降解机理, 优化活性污泥体系有重要意义。
将组装 contigs 与 KEEG 数据库进行比对, 共注释到 87 个功能基因(xbna 附录 2), 参与有机污染物的降解。根据有机污染物的结构, 将降解基因分为六大类, 分别为单环芳烃、多环芳烃、杂环芳烃、烷烃、脱卤酶和其他类别, 约有 53.99%的降解基因参与单环芳烃化合物的代谢, 进一步将单环芳烃降解基因分为芳香羧酸、芳香醇、芳香烃、芳香醛、芳香酮、氯化芳香化合物和苯胺类(图 6)。在垃圾渗滤液活性污泥中, 芳香羧酸类降解基因的种类最多, 丰度最高 (35899 hits), 包括苯甲酸双加氧酶(808 hits)、对羟基苯甲酸单加氧酶(324 hits)、邻苯二甲酸 4,5-双加氧酶(304 hits)、4,5-二羟基邻苯二甲酸脱羧酶(131 hits)和 4-羟基苯乙酸 3-单加氧酶(242 hits)。芳香醇类降解基因的丰度也较高, 包括苯酚单加氧酶(221 hits)、芳醇脱氢酶(242 hits)和4-甲酚脱氢酶(538 hits)。芳香烃类主要为甲苯单加氧酶系统蛋白, 在体系中丰度较低。芳香醛类主要为苯乙醛脱氢酶(200 hits), 芳香酮类主要包括 4-羟基苯乙酮单加氧酶(120 hits)和2,4'-二羟基苯乙酮双加氧酶(30 hits), 苯胺类主要为二甲基苯胺单加氧酶(51 hits)。
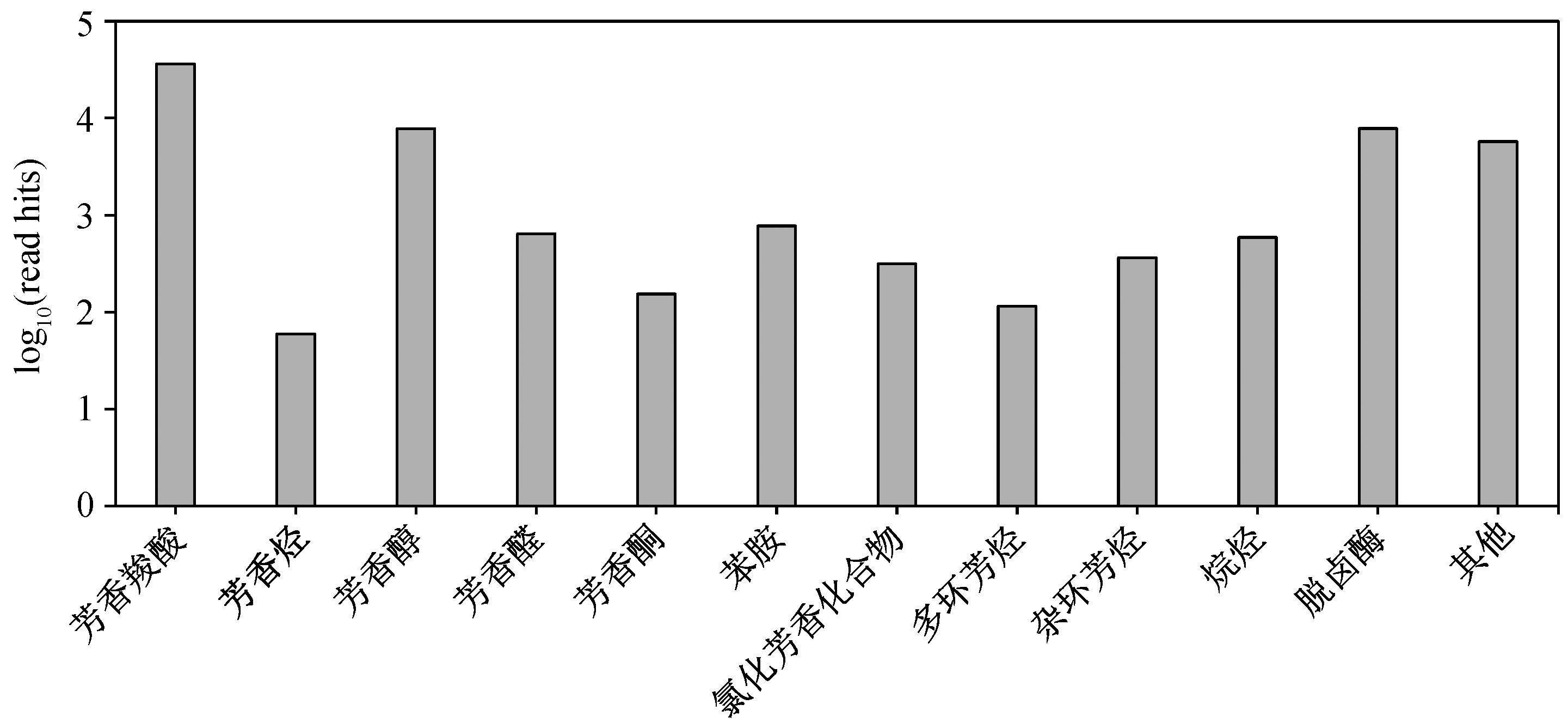
图6 有机污染物降解基因种类及丰度
Fig. 6 Abundances of various organic pollutant degrading genes
与单环芳烃类降解基因相比, 多环芳烃和杂环芳烃降解基因种类较少, 丰度较低。多环芳烃中发现与萘降解相关的萘 1,2-加氧酶铁氧还原蛋白还原酶(55 hits), 没有发现与蒽、菲等复杂的多环芳烃代谢相关的基因, 与杂环芳烃污染物降解相关的有咔唑 1,9a-双加氧酶(6 hits)、5-(羟甲基)糠醛/糠醛氧化酶(169 hits)、2-吡喃酮-4,6-二羧酸乳糖酶(121 hits)和羟基喹啉 1,2-加氧酶(65 hits), 说明垃圾渗滤液活性污泥对结构复杂的多环芳烃和杂环芳烃降解的潜力较低。除芳香族化合物外, 体系中还发现与烷烃降解相关的烷烃 1-单加氧酶(591 hits), 未发现与烯烃降解相关的基因。与有机卤化合物降解相关的 2-卤酸脱卤酶(6381 hits)和卤乙酸脱卤酶(776 hits)在体系中丰度较高, 说明活性污泥对垃圾渗滤液有机卤化合物的降解具有较大的潜力。
为了解不同类型污水处理厂活性污泥降解基因的差异, 将本研究的数据集(Leachate)与其他 3 个宏基因组数据集(分别来自印度的市政污水处理厂(AERA)[48]、丹麦的增强生物除磷处理厂(EBPR)[49]和中国的制革厂废料处理厂(Tannery)[50])进行比较。由图 7 可知, 垃圾渗滤液处理厂的活性污泥具有的降解基因种类最多, 制革厂和污水处理厂次之,EBRP 处理厂最少, 说明污染物降解基因的丰富度与废水的成分有很大的关系, 微生物发挥的功能与污水处理系统中存在的可降解底物息息相关。Masoner 等[51]研究美国 19 个垃圾填埋场的垃圾渗滤液,检测到 129 种难降解有机污染物, 如萘和菲等多环芳香族化合物、氯化芳香族化合物、磷酸酯、邻苯二甲酸酯、酚类化合物以及苯胺类化合物等。其中, 苯酚、双酚 A 和 4-羟基甲苯等的检出频率高于 50%, 检出浓度高达 mg/L 级别, 比普通污水处理厂的检出浓度高几个数量级, 因此, 相对于普通的废水, 其降解基因具有更高的多样性。
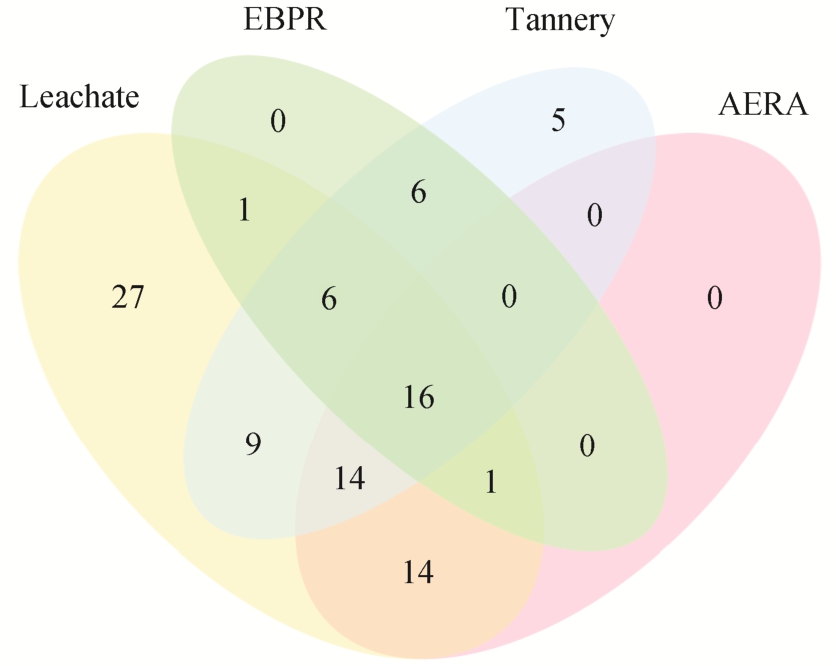
图7 4 种污水处理厂有机污染物降解基因种类多样性
Fig. 7 Diversity of organic pollutant degradation genes in four wastewater treatment plants
4 种废水处理厂活性污泥中共有的有机污染物降解酶包括 4-羟基苯乙酸 3-单加氧酶、水杨酸羟化酶、原儿茶酸 3,4-双加氧酶 β 亚基、原儿茶酸 4,5-双加氧酶 β 链、均龙胆酸 1,2-双加氧酶、龙胆酸1,2-双加氧酶、苯乙醛脱氢酶和烷烃 1-单加氧酶等(xbna 附录 3), 说明这些酶作用的化合物在污水处理系统中普遍存在。例如, 水杨酸、原儿茶酸和龙胆酸是芳香化合物生物降解的中间产物[52]在污水处理系统中广泛存在, 因此在不同的污水处理体系中都发现相应的降解酶。
垃圾渗滤液处理厂的活性污泥中存在大量特有的降解酶, 如杂环芳烃降解酶(咔唑 1,9a-双加氧酶、5-(羟甲基)糠醛/糠醛氧化酶和 2,5-呋喃二甲酸脱羧酶)、芳香羧酸类降解酶(邻苯二甲酸 4,5-双加氧酶、4-羟基苯甲酸脱羧酶亚基 C、4-甲氧基苯甲酸单加氧酶和(S)-扁桃酸脱氢酶)、苯胺类降解酶(邻氨基苯甲酸 1,2-双加氧酶)、苯酮类降解酶(4-羟基苯乙酮单加氧酶)以及卤代烷烃脱卤酶等(xbna 附录 3), 这些酶的作用化合物是生产医药、纤维、包装材料、塑料和其他日用品的原材料[53], 经废弃物填埋后进入垃圾渗滤液中, 长期富集后形成垃圾渗滤液活性污泥独特的降解酶体系。
2) 有机污染物降解基因的分布。
通过对不同类群微生物的功能注释, 确定不同门水平微生物降解有机污染物的功能差异(图 8)。在 18 个细菌门中发现有机污染物降解基因, 而在古菌 Nanoarchaeota 中未注释到降解基因, 说明细菌是垃圾渗滤液活性污泥中有机物降解的功能微生物。
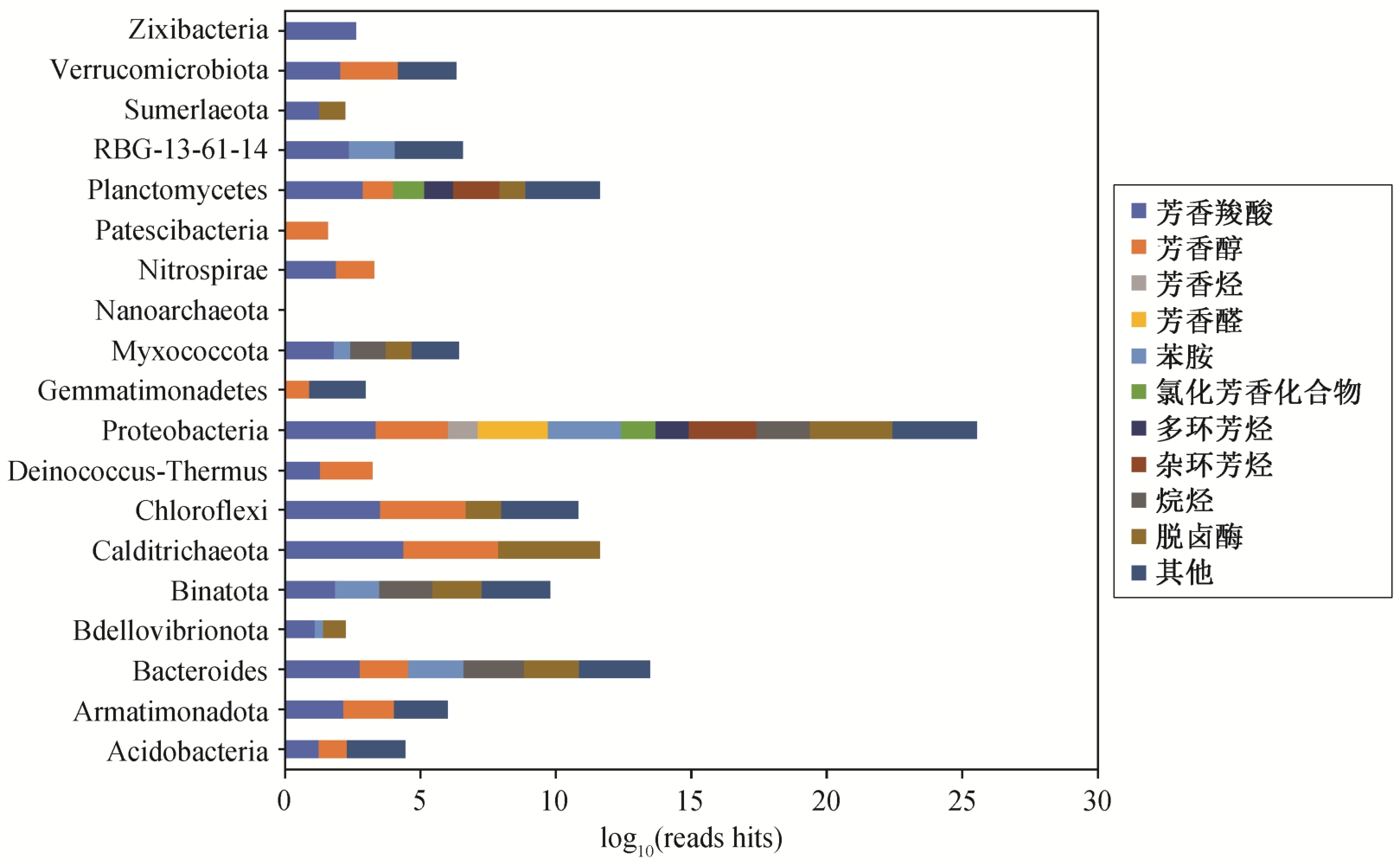
图8 不同门水平微生物有机污染物降解基因多样性及丰度
Fig. 8 Diversity and abundances of organic pollutant degrading genes in microorganisms at different phylum levels
18 个细菌门中, 有机污染物降解基因在种类和丰度上存在很大的差别, Proteobacteria 是体系中有机污染物降解的优势菌门, 降解基因种类最多, 丰度最高, 在总的有机物降解基因中占 12.82%, 在Proteobacteria 中还发现独特的降解基因(如苯/甲苯/氯苯双加氧酶、苯甲醛脱氢酶和苯乙醛脱氢酶),说明 Proteobacteria 在垃圾渗滤液难降解有机污染物的去除方面可能发挥着关键作用。
Bacteroidetes, Planctomycetes, Calditrichaeota和 Choroflexi 门也是体系中有机物降解的重要功能微生物。Bacteroidetes 注释到芳香羧酸类、芳香醇类、苯胺、烷烃、有机卤化合物降解的功能基因,其中, 二甲基苯胺单加氧酶仅在 Bacteroidetes 微生物中发现。Planctomycetes 在降解氯化芳香化合物、多环芳烃和杂环芳烃类化合物方面具有优势,如 5-(羟甲基)糠醛和四氯苯醌, 说明 Planctomycetes对复杂的芳香化合物的降解具有很大潜力。Calditrichaeota 和 Choroflexi 中芳香羧酸类降解基因最高,这两个门中存在大量的龙胆酸 1,2-双加氧酶、均龙胆酸 1,2-双加氧酶和儿茶酚 2,3-双加氧酶, 这些酶催化芳香族化合物苯环的开环反应, 污染物经开环后进一步代谢进入三羧酸循环(TCA circle), 降解产物被微生物用于合成自身的生物量, 同时产生 CO2和 H2O, 因此 Calditrichaeota 和 Choroflexi 对芳香化合物的彻底氧化分解具有重要意义。
3 结论
本研究利用 16S rRNA 基因和宏基因组测序技术, 探究垃圾渗滤液处理系统活性污泥的种群结构和功能特征, 共鉴定出 32 个门, 334 个属。Calditrichaeota 门和 Calorithrix 属分别为优势菌门和属,这是关于污水处理系统中 Calditrichaeota 门和 Calorithrix 属的首次报道。活性污泥中存在硝化、反硝化、同化硝酸盐还原、异化硝酸盐还原和氮固定 5 条氮循环途径, 反硝化相关基因是丰度最高的脱氮功能基因, 主要分布于 Calditrichaeota, Proteobacteria 和 Choroflexi 门。活性污泥中含有丰富的难降解有机污染物降解基因, 远高于工业废水和市政污水处理厂的活性污泥, 其中 Proteobacteria, Bacteroidetes, Planctomycetes, Calditrichaeota 和 Choroflexi是主要的有机物降解功能微生物。
[1] Qi Chengdu, Huang Jun, Wang Bin, et al. Contaminants of emerging concern in landfill leachate in China: a review. Emerging Contaminants, 2018, 4: 1–10
[2] 张胜利. 基于垃圾渗滤液中有机污染物特征的预处理研究[D]. 成都: 西南交通大学, 2010
[3] Andrews W J, Masoner J R, Cozzarelli I M. Emerging contaminants at a closed and an operating landfill in Oklahoma. Groundwater Monitoring & Remediation,2012, 32(1): 120–130
[4] Clarke B O, Anumol T, Barlaz M, et al. Investigating landfill leachate as a source of trace organic pollutants. Chemosphere, 2015, 127: 269–275
[5] Tran N H, Hu J Y, Ong S L. Simultaneous determination of PPCPs, EDCs, and artificial sweeteners in environmental water samples using a single-step SPE coupled with HPLC–MS/MS and isotope dilution.Talanta, 2013, 113: 82–92
[6] Tran N H, Urase T, Ngo H H, et al. Insight into metabolic and cometabolic activities of autotrophic and heterotrophic microorganisms in the biodegradation of emerging trace organic contaminants. Bioresource Technology, 2013, 146(10): 721–731
[7] 宁欣强. A+OSA 污泥减量工艺微生物群落结构及代谢特征研究[D]. 重庆: 重庆大学, 2015
[8] Zhang Bo, Yu Quanwei, Yan Guoqi, et al. Seasonal bacterial community succession in four typical wastewater treatment plants: correlations between core microbes and process performance. Scientific Reports,2018, 8: no4566
[9] Fang Hua, Zhang Houpu, Han Lingxi, et al. Exploring bacterial communities and biodegradation genes in activated sludge from pesticide wastewater treatment plants via metagenomic analysis. Environmental Pollution, 2018, 243: 1206–1216
[10] Joshi D R, Zhang Y, Gao Y X, et al. Biotransformation of nitrogen-and sulfur-containing pollutants during coking wastewater treatment: correspondence of performance to microbial community functional structure. Water Research, 2017, 121: 338–348
[11] Andrews S. FastQC: a quality control tool for high throughput sequence data [EB/OL]. (2010) [2019–09–01]. https://www.bioinformatics.babraham.ac.uk/pro jects/fastqc/
[12] Bolger A M, Lohse M, Usadel B. Trimmomatic: a flexible trimmer for Illumina sequence data. Bioinformatics, 2014, 30(15): 2114–2120
[13] Caporaso J G, Kuczynski J, Stombaugh J, et al.QIIME allows analysis of high-throughput community sequencing data. Nat Methods, 2010, 7(5): 335–336
[14] Pruesse E, Quast C, Knittel K, et al. SILVA: a comprehensive online resource for quality checked and aligned ribosomal RNA sequence data compatible with ARB. Nucleic Acids Res, 2007, 35(21): 7188–7196
[15] Bankevich A, Nurk S, Antipov D, et al. SPAdes: a new genome assembly algorithm and its applications to single-cell sequencing. Journal of Computational Biology, 2012, 19(5): 455–477
[16] Langmead B, Salzberg S L. Fast gapped-read alignment with Bowtie 2. Nature Methods, 2012, 9(4):357–359
[17] Wu Yuwei, Simmons B A, Singer S W. MaxBin 2.0:an automated binning algorithm to recover genomes from multiple metagenomic datasets. Bioinformatics,2016, 32(4): 605–607
[18] Kang D D, Froula J, Egan R, et al. MetaBAT, an efficient tool for accurately reconstructing single genomes from complex microbial communities. Peer J, 2015, 3(8): no1165
[19] Johannes A, Brynjar S B, Ino D B, et al. Binning metagenomic contigs by coverage and composition.Nature Methods, 2014, 11(11): 1144–1146
[20] Parks D H, Imelfort M, Skennerton C T, et al.CheckM: assessing the quality of microbial genomes recovered from isolates, single cells, and metagenomes. Genome Res, 2015, 25(7): 1043–1055
[21] Parks D H, Rinke C, Chuvochina M, et al. Recovery of nearly 8,000 metagenome-assembled genomes substantially expands the tree of life. Nature Microbiology, 2017, 2(11): 1533–1542
[22] Parks D H, Chuvochina M, Waite D W, et al. A standardized bacterial taxonomy based on genome phylogeny substantially revises the tree of life. Nature Biotechnology, 2018, 36(10): 996–1004
[23] Hyatt D, Chen G L, Locascio P F, et al. Prodigal:prokaryotic gene recognition and translation initiation site identification. BMC Bioinformatics, 2010, 11(1):no119
[24] Altschul S F. Basic local alignment search tool(BLAST). Journal of Molecular Biology, 2012, 215(3): 403–410
[25] Mukherjee S, Juottonen H, Siivonen P, et al. Spatial patterns of microbial diversity and activity in an aged creosote-contaminated site. The ISME Journal, 2014,8(10): 2131–2142
[26] Ibekwe A M, Ma J, Murinda S E. Bacterial community composition and structure in an Urban River impacted by different pollutant sources. Science of the Total Environment, 2016, 566: 1176–1185
[27] Ma Qiao, Qu Yuanyuan, Shen Wenli, et al. Bacterial community compositions of coking wastewater treatment plants in steel industry revealed by Illumina high-throughput sequencing. Bioresource Technology,2015, 179: 436–443
[28] Nikolaivits E, Dimarogona M, Fokialakis N, et al.Marine-derived biocatalysts: importance, accessing,and application in aromatic pollutant bioremediation.Frontiers in Microbiology, 2017, 8: 265
[29] Zhang Bo, Xu Xiangyang, Zhu Liang. Structure and function of the microbial consortia of activated sludge in typical municipal wastewater treatment plants in winter. Scientific Reports, 2017, 7(1): 1–11
[30] Fang Dexin, Zhao Gen, Xu Xiaoyi, et al. Microbial community structures and functions of wastewater treatment systems in plateau and cold regions. Bioresource Technology, 2018, 249: 684–693
[31] Li Xiaoran, Du Bing, Fu Haixia, et al. The bacterial diversity in an anaerobic ammonium-oxidizing (anammox) reactor community. Systematic & Applied Microbiology, 2009, 32(4): 278–289
[32] Hugenholtz P, Tyson G W, Blackall L L, et al.Filamentous Chloroflexi (green non-sulfur bacteria)are abundant in wastewater treatment processes with biological nutrient removal. Microbiology, 2002, 148(8): 2309–2318
[33] Zhao Yunpeng, Liu Shufeng, Jiang Bo, et al. Genomecentered metagenomics analysis reveals the symbiotic organisms possessing ability to cross-feed with anammox bacteria in anammox consortia. Environmental Science & Technology, 2018, 52(19): 11285–11296
[34] Guo Jianhua, Peng Yongzhen, Ni Bingjie, et al. Dissecting microbial community structure and methaneproducing pathways of a full-scale anaerobic reactor digesting activated sludge from wastewater treatment by metagenomic sequencing. Microbial Cell Factories,2015, 14: no33
[35] Sievert S M, Kueve R J, Muyzer G. Identification of 16S ribosomal DNA-defined bacterial populations at a shallow submarine hydrothermal vent near Milos Island (Greece). Appl Environ Microbiol, 2000, 66(7):3102–3109
[36] Margarita L M, Nadezhda A K, Nikolai A C, et al.Caldithrix abyssi gen. nov. sp. nov. a nitrate-reducing,thermophilic, anaerobic bacterium isolated from a Mid-Atlantic Ridge hydrothermal vent, represents a novel bacterial lineage. International Journal of Systematic and Evolutionary Microbiology, 2003, 53(1):323–329
[37] Kompantseva E I, Kublanov I V, Perevalova A A, et al. Calorithrix insularis gen. nov. sp. nov. a novel representative of the phylum Calditrichaeota. International Journal of Systematic and Evolutionary Microbiology, 2016, 67(5): 1486–1490
[38] Marshall I P G, Starnawski P, Cupit C, et al. The novel bacterial phylum Calditrichaeota is diverse,widespread and abundant in marine sediments and has the capacity to degrade detrital proteins. Environmental Microbiology Reports, 2017, 9(4): 397–403
[39] Kublanov I V, Sigalova O M, Gavrilov S N, et al.Genomic analysis of Caldithrix abyssi, the thermophilic anaerobic bacterium of the novel bacterial phylum Calditrichaeota. Frontiers in Microbiology, 2017, 8(75): 195–195
[40] Luo Hongwei, Zeng Yifeng, Cheng Ying, et al. Recent advances in municipal landfill leachate: a review focusing on its characteristics, treatment, and toxicity assessment. Science of the Total Environment, 2019,703: 135468
[41] Ransom-Jones E, Mccarthy A J, Haldenby S, et al.Lignocellulose-degrading microbial communities in landfill sites represent a repository of unexplored biomass-degrading diversity. Msphere, 2017, 2(4):e00300-17
[42] Wang Yingmu, Lin Ziyuan, He Lei, et al. Simultaneous partial nitrification, anammox and denitrification(SNAD) process for nitrogen and refractory organic compounds removal from mature landfill leachate:performance and metagenome-based microbial ecology. Bioresource Technology, 2019, 294: no122166
[43] 王晓慧. 城市污水处理厂中氨氧化菌及细菌群落结构与功能研究[D]. 北京: 清华大学, 2010
[44] Yu Ke, Zhang Tong. Metagenomic and metatranscriptomic analysis of microbial community structure and gene expression of activated sludge. Plos One,2012, 7(5): e38183
[45] 田美, 刘汉湖, 申欣. 基于新一代测序技术的 A2O与 BIOLAK 活性污泥宏基因组比较分析. 环境科学,2016, 37(2): 638–646
[46] 彭永臻, 钱雯婷, 王琦, 等. 基于宏基因组的城市污水处理厂生物脱氮污泥菌群结构分析. 北京工业大学学报, 2019, 45(1): 99–106
[47] Sui Qian, Zhao Wentao, Cao Xuqi, et al. Pharmaceuticals and personal care products in the leachates from a typical landfill reservoir of municipal solid waste in Shanghai, China: Occurrence and removal by a fullscale membrane bioreactor. Journal of Hazardous Materials, 2017, 323: 99–108
[48] More R P, Mitra S, Raju S C, et al. Mining and assessment of catabolic pathways in the metagenome of a common effluent treatment plant to induce the degradative capacity of biomass. Bioresource Technology, 2014, 153: 137–146
[49] Albertsen M, Hansen L B, Saunders A M, et al. A metagenome of a full-scale microbial community carrying out enhanced biological phosphorus removal.The ISME Journal, 2012, 6(6): 1094–1106
[50] Wang Zhu, Zhang Xuxiang, Huang Kailong, et al.Metagenomic profiling of antibiotic resistance genes and mobile genetic elements in a tannery wastewater treatment plant. Plos One, 2013, 8(10): e76079
[51] Masoner J R, Kolpin D W, Furlong E T, et al.Contaminants of emerging concern in fresh leachate from landfills in the conterminous United States.Environmental Science: Processes & Impacts, 2014,16(10): 2335–2354
[52] 申国兰, 李利, 陈莎. 微生物降解石油源多环芳香烃的研究进展. 土壤, 2018, 50(1): 16–27
[53] 周晨, 龚党生, 李学敏, 等. 2,5-呋喃二甲酸的合成研究进展及其应用前景. 染料与染色, 2018, 55(2):38–42