研究简报
城镇污水处理系统中4种抗生素抗性基因的沿程变化
城镇污水处理系统中4种抗生素抗性基因的沿程变化
包樱钰1 谢辉2 陈吕军2 温东辉1,†
1.北京大学环境科学与工程学院, 北京 100871; 2.清华大学环境学院, 北京 100084; †通信作者, E-mail: dhwen@pku.edu.cn
摘要 为探究抗生素抗性基因(ARGs)在城镇污水处理系统中的沿程变化, 针对 4 种关注度较高的 ARGs (sulII, ermB, tetC和blaPSE-1)和 I 型整合子的整合酶基因(intI1), 选取京津冀地区一座中小城镇的污水处理厂, 使用普通 PCR 和实时荧光定量 PCR 技术, 对各工艺单元的水样进行细胞内 ARGs 和 intI1 的定性及定量检测分析。结果表明, 4 种 ARGs 和 intI1 普遍存在于城镇污水处理系统中, 出水中 ARGs 和 intI1 的绝对丰度降低, 去除量在 1.26~2.30logs 之间。相关性分析表明, intI1 和水质因子(pH, COD和NH3-N)可能与 4 种 ARGs 的传播扩散有关。
关键词 抗生素抗性基因(ARGs); 城镇污水处理系统; A2/O工艺; 实时荧光定量PCR
由于环境选择压力(抗生素、重金属等)的存在, 抗生素抗性基因(antibiotic resistance genes, ARGs)得以迅速在环境中产生与传播[1]。与化学污染物不同, ARGs 具有遗传复制、水平转移(horizontal gene transfer, HGT)等生物学特性[2–3], 一旦进入环境就很难控制和消除。因此, 近年来 ARGs 成为备受瞩目的一种新型污染物。研究表明, ARGs 在常规的城镇污水处理厂进、出水中普遍存在[4–5]。城镇污水处理系统中的抗生素、重金属、可移动遗传元件(mobile genetic elements, MGEs)和微生物等可能对ARGs 的形成、水平转移和扩散起到促进作用[6]。因此, 对城镇污水处理厂中 ARGs 赋存特征和去除效果展开研究十分必要。
京津冀地区是我国北方经济的重要核心区, 人口密集, 是抗生素排放强度较大的区域之一[7], 存在潜在的 ARGs 污染风险。本研究选取京津冀地区典型中小城镇的污水处理厂, 采集沿程各工艺单元水样进行 ARGs 的定量检测分析, 揭示城镇污水处理过程中 ARGs 的赋存情况, 为京津冀地区 ARGs污染的防控提供参考。
1 ARGs 和基本理化指标的测定
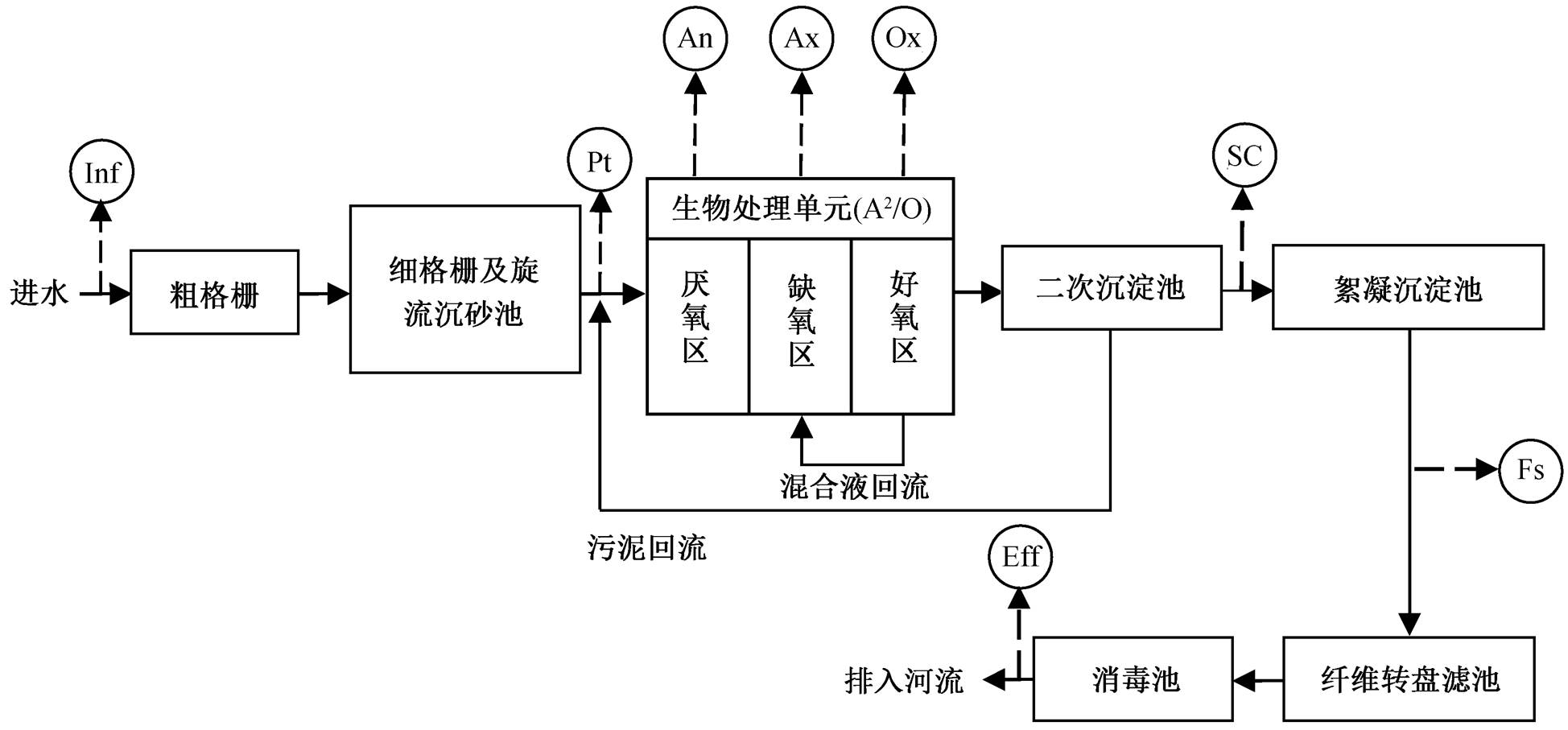
选取河北省一座生活污水处理厂为研究对象, 图 1 展示其污水处理工艺流程及采样点位(圆圈表示)。样品采集后, 立即进行理化指标和 ARGs 的定量分析。分别采用电极法[8]、重铬酸盐法[8]、纳氏试剂分光光度法[8]和钼酸铵分光光度法[8]测定样品的 pH, COD, NH3-N 和 TP, 结果见表 1。对样品进行 DNA 提取后, 使用普通 PCR 和实时荧光定量PCR(qPCR)的 SYBR Green I 方法, 对 sulII, tetC, ermB 和 blaPSE-1 4 种 ARGs 以及 I 型整合子的整合酶基因 intI1 分别进行定性和定量分析, 操作流程见文献[9]。此外, 对 16S rDNA 进行定量测定, 作为微生物总量的表征值。
表1 样品理化指标分析结果
Table 1 Physicochemical analysis results
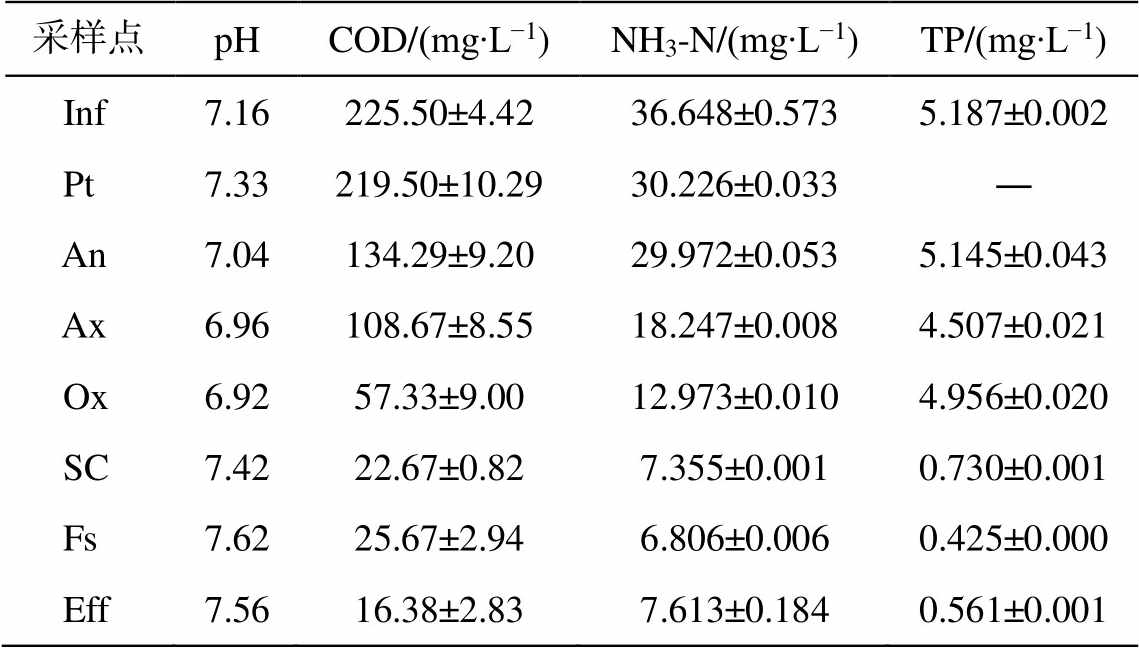
采样点pHCOD/(mg∙L−1)NH3-N/(mg∙L−1)TP/(mg∙L−1) Inf7.16225.50±4.4236.648±0.5735.187±0.002 Pt7.33219.50±10.2930.226±0.033― An7.04134.29±9.2029.972±0.0535.145±0.043 Ax6.96108.67±8.5518.247±0.0084.507±0.021 Ox6.9257.33±9.0012.973±0.0104.956±0.020 SC7.4222.67±0.827.355±0.0010.730±0.001 Fs7.6225.67±2.946.806±0.0060.425±0.000 Eff7.5616.38±2.837.613±0.1840.561±0.001
说明: ―表示未测定。
2 结果与讨论
2.1 污水处理系统中ARGs 的分布特征
2.1.1 ARGs绝对丰度
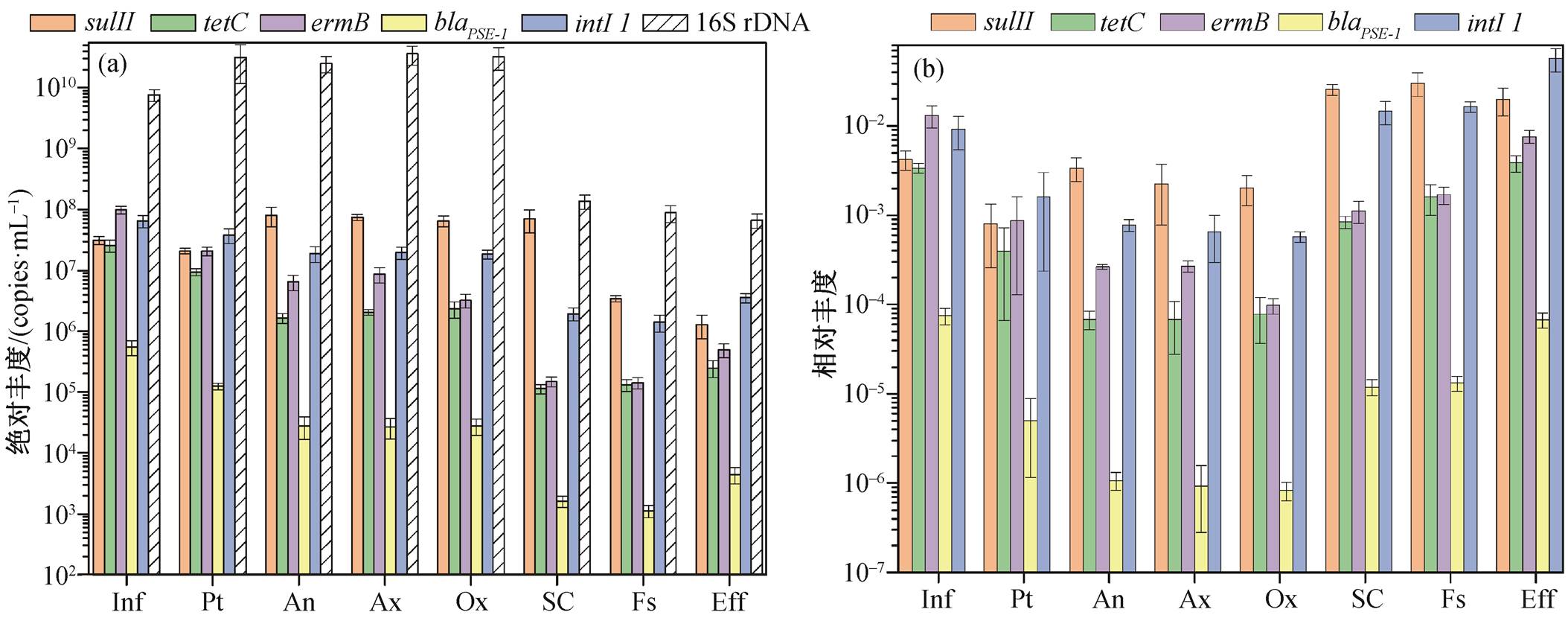
图 2(a)显示目标基因在污水处理系统各单元中的分布情况, 4 种 ARGs 和 intI1 在全部水样中均有检出, 表明它们普遍存在于污水处理系统中。总进水中 ermB 的绝对丰度最高, 目标基因绝对丰度分布在 5.50×105~9.93×107copies/mL 之间。ermB, tetC, blaPSE-1 和 intI1 的绝对丰度沿处理工艺流程大致呈降低趋势。消毒工艺出水中 ermB, tetC, blaPSE-1 和intI1 的绝对丰度显著升高, 与 Yoon 等[10]的研究结果一致。
进入 A2/O 处理单元后, sulII 的绝对丰度显著升高, 在厌氧区达到最大值。经过二次沉淀, sulII 的绝对丰度进一步增加, 是绝对丰度最高的 ARGs; 经过絮凝沉淀和消毒后, 出水中 sulII 的绝对丰度显著降低。
在总出水中, 目标基因的绝对丰度排序为 intI1> sulII > ermB > tetC > blaPSE-1, 在 3.40×103~3.05×106copies/mL 之间, 所有 ARGs 和 intI1 在出水中的绝对丰度显著低于进水。
2.1.2 ARGs相对丰度
图 2(b)显示目标基因在污水处理系统各单元中的相对丰度(即目标基因与 16S rDNA 拷贝数之比)。对比图 2(a)与(b)可知, ARGs 及 intI1在绝对丰度和相对丰度上的变化趋势不同。这是由单位体积水样的微生物量差异引起的[11], 仅关注绝对丰度无法体现 ARGs 在微生物基因组中的占比情况, 因此对ARGs 及 intI1 的相对丰度进行分析十分必要。
总进水中各目标基因的相对丰度在 10−5~10−2之间, 与绝对丰度结果一致, 进水中相对丰度最高的为 ermB。ermB, tetC, blaPSE-1 与 intI1 的相对丰度变化趋势大致相同: 经过细格栅和旋流沉砂池、A2/O 各处理阶段, 上述基因在微生物群落基因组中的占比逐渐下降; 经过二次沉淀、絮凝沉淀和消毒后, 相对丰度呈上升趋势。sulII 相对丰度的变化趋势与上述基因有较大的差异。在 A2/O 的厌氧区中, sulII 相对丰度升高。经过二次沉淀和絮凝沉淀, sulII 相对丰度呈上升趋势。消毒处理后, sulII 相对丰度降低, 但仍显著高于总进水。
总出水中, 目标基因的相对丰度分布在 6.76× 10−5~5.71×10−2之间, sulII, tetC 和 intI1 的相对丰度高于进水, 说明污水处理后, 这几类基因在微生物群落基因组中的占比增大。有研究证明, 污水处理系统是受纳水体下游 ARGs 的主要来源[12–13], 因此城镇污水处理系统对于受纳地表水的ARGs输入及其生态风险不容小觑。
2.2 污水处理系统对 ARGs 和 intI1 的去除效果
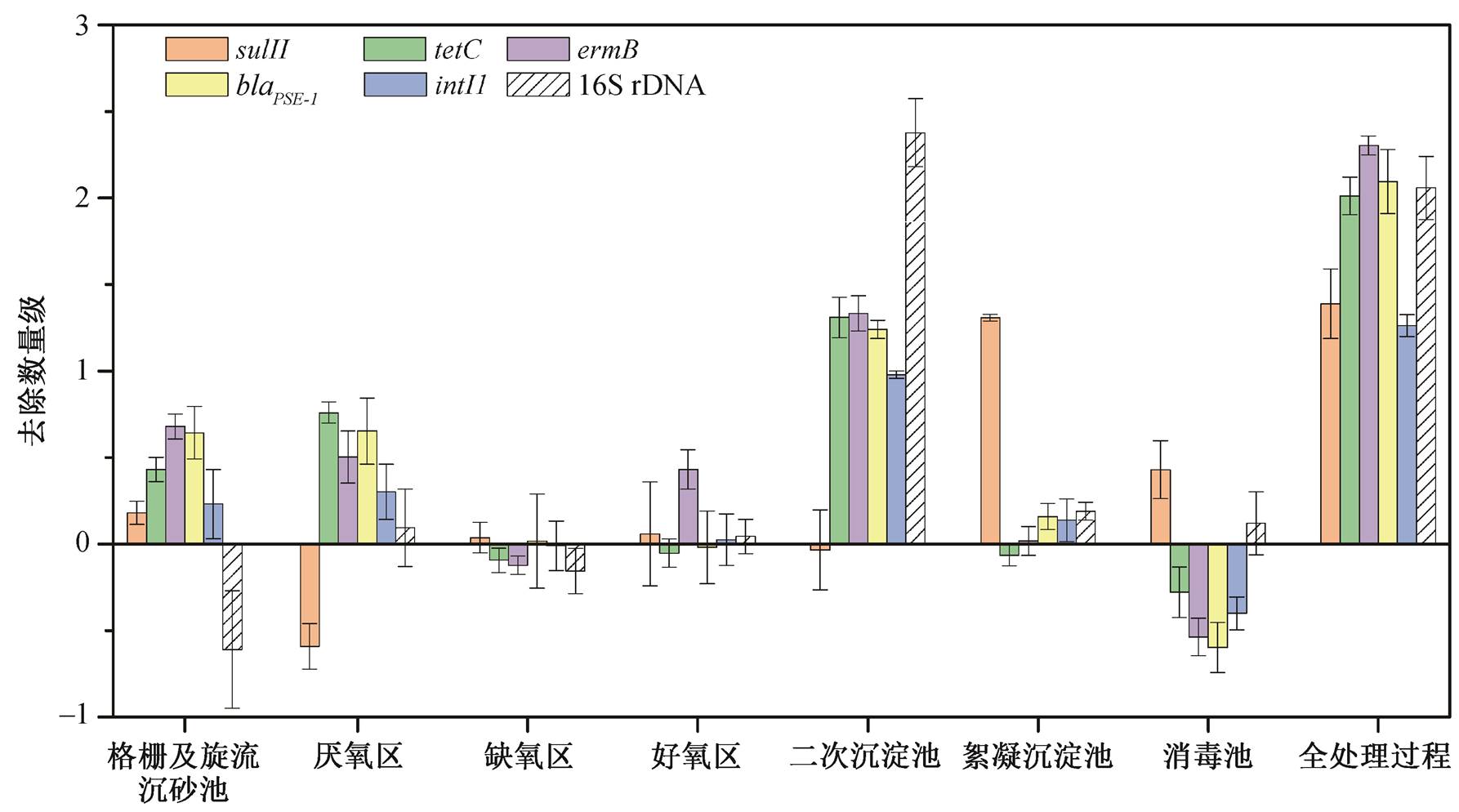
图 3 显示各污水处理单元及污水处理全程对目标基因的去除情况。不同工艺单元对各目标基因的去除效果有明显差异, 且存在去除量为负的现象。生物处理单元中微生物群落的变化可能是导致本研究中 ARGs 去除或富集效果各异的重要原因[14]。Xu 等[15]和 Börjesson 等[16]认为, 二沉池内 ARGs 附着在生物质上, 并随之脱离液相进入污泥中, 使水相中的 ARGs 减少。剩余污泥的外运是 ARGs 进入自然环境的潜在途径[6,17], 因此对剩余污泥的合理处置是十分必要的。ClO2 消毒仅对 sulII 和微生物总量有一定的削减作用, 不能有效地控制其他目标基因。经过全部工艺后, 目标基因的削减量在1.26~2.30logs 之间, 顺序为: ermB > blaPSE-1 > tetC > sulII > intI1。
2.3 相关性分析
2.3.1目标基因之间的相关性
表 2 列出目标基因绝对丰度之间的相关性分析结果。intI1 与 ermB, tetC, blaPSE-1 之间均存在显著的正相关关系(P<0.001)。intI1 是 I 型整合子中编码整合酶的基因, 整合子几乎存在于各种可移动遗传元件和染色体上, 与 ARGs 在环境中的传播、扩散联系十分紧密[18–19]。I 型整合子可能是这几类抗性基因传播扩散的重要机制。
2.3.2水质因子与目标基因的相关性
表 3 列出水质因子与目标基因之间的相关性分析结果。结果表明, sulII 和微生物总量分别与pH 显著负相关(P<0.05), 4 个目标基因(tetC, ermB, blaPSE-1 和 intI1)分别与两个水质因子(COD 和 NH3-N)之间呈显著的正相关关系(P<0.05), 总 ARGs 与NH3-N 显著正相关(P<0.05), 微生物总量与 TP 显著正相关(P<0.01)。Nõlvak 等[20]、奚慧[21]和杜雪[22]的研究结果分别表明 ARGs 与 pH, NH3-N 及 COD 之间正相关, 本文结果与之一致, 可能的原因为碳、氮和磷等营养元素促进微生物的生长繁殖, 从而有助于 ARGs 的扩散[23]。上述研究结果说明对污水处理厂基本水质指标(pH, COD 和 NH3-N 等)的监测可能有助于预测 ARGs 的丰度水平, 可为揭示污水处理系统的 ARGs 污染风险提供帮助。
表2 目标基因之间的相关性分析
Table 2 Correlation between the target genes’ absolute abundances
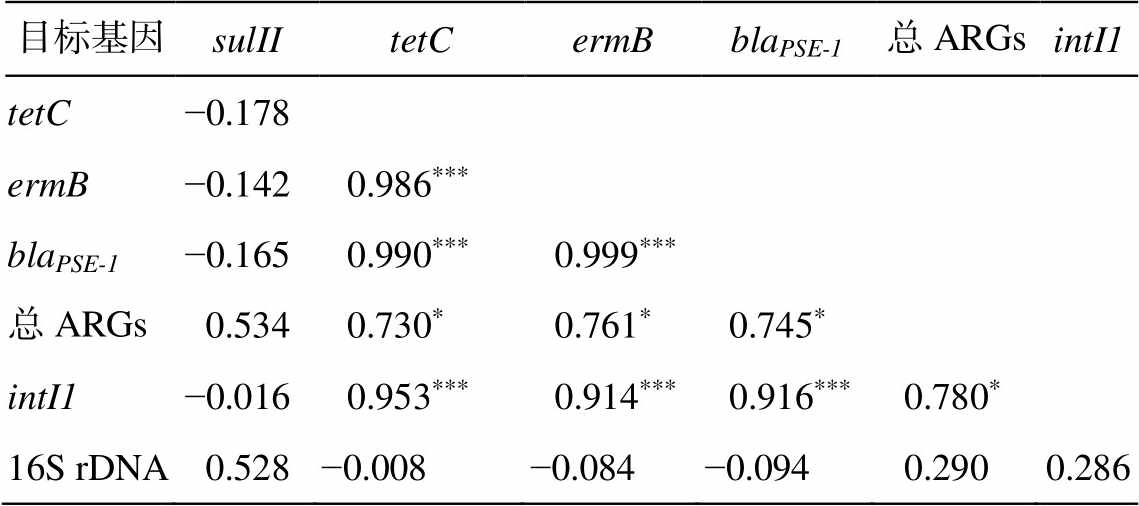
目标基因sulIItetCermBblaPSE-1总ARGsintI1 tetC−0.178 ermB−0.142 0.986*** blaPSE-1−0.165 0.990*** 0.999*** 总ARGs0.534 0.730* 0.761* 0.745* intI1−0.016 0.953*** 0.914*** 0.916*** 0.780* 16S rDNA0.528 −0.008 −0.084 −0.094 0.2900.286
注: ***表示在0.001(双侧)水平上显著相关, **表示在 0.01(双侧)水平上显著相关, *表示在0.05 (双侧)水平上显著相关, 下同。
表3 水质因子与目标基因之间的相关性分析
Table 3 Correlation between the target genes’ absolute abundances and water quality factors
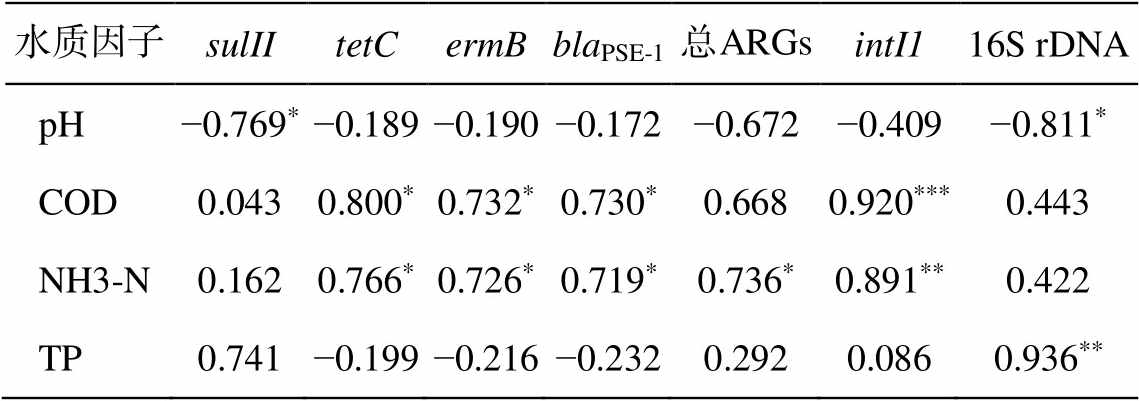
水质因子sulIItetCermBblaPSE-1总 ARGsintI116S rDNA pH−0.769*−0.189−0.190−0.172−0.672−0.409−0.811* COD0.0430.800*0.732*0.730*0.6680.920***0.443 NH3-N0.1620.766*0.726*0.719*0.736*0.891**0.422 TP0.741−0.199−0.216−0.2320.2920.0860.936**
3 结论
本研究采集一座中小型生活污水处理厂中各工艺单元水样, 进行 4 种 ARGs 的定性和定量检测分析, 揭示城镇污水处理过程中 ARGs 的分布和变化规律, 得到如下结论。
1) sulII, ermB, tetC, blaPSE-1 与 I 型整合子普遍存在于城镇污水处理系统中。进水中 ermB 的绝对和相对丰度最高, 出水中 intI1 的绝对和相对丰度最高。总出水中目标基因的绝对丰度分布在 3.40×103 ~3.05×106copies/mL 之间, 相对丰度分布在 6.76× 10−5~ 5.71×10−2之间。
2)污水处理降低 4 种 ARGs 和 I 型整合子的绝对丰度(去除量在 1.26~2.30logs 之间), 提高sulII, tetC和intI1的相对丰度。
3)相关性分析表明, ermB, tetC 和 blaPSE-1 之间以及 I 型整合子与 ermB, tetC, blaPSE-1 之间均存在显著的正相关关系(P<0.0001); pH, COD 和 NH3-N 等水质因子与 ARGs、I 型整合子和微生物量之间存在一定的相关性(P<0.005)。
参考文献
[1] Sharma V K, Johnson N, Cizmas L, et al. A review of the influence of treatment strategies on antibiotic resistant bacteria and antibiotic resistance genes. Chemosphere, 2016, 150(70): 2–14
[2] Zhang X X, Zhang T, Fang H. Antibiotic resistance genes in water environment. Appl Microbiol Bio-technol, 2009, 82(3): 397–414
[3] 罗义, 周启星. 抗生素抗性基因(ARGs) —— 一种新型环境污染物. 环境科学学报, 2008, 28(8): 13–19
[4] Wen Qinxue, Yang Lian, Duan Ruan, et al. Monito-ring and evaluation of antibiotic resistance genes in four municipal wastewater treatment plants in Harbin, Northeast China. Environmental Pollution, 2016, 212: 34–40
[5] Mcconnell M M, Truelstrup Hansen L, Jamieson R C, et al. Removal of antibiotic resistance genes in two tertiary level municipal wastewater treatment plants. Science of the Total Environment, 2018, 643: 292–300
[6] Guo Jianhua, Li Jie, Chen Hui, et al. Metagenomic analysis reveals wastewater treatment plants as hot-spots of antibiotic resistance genes and mobile genetic elements. Water Research, 2017, 123(4): 68–78
[7] Zhang Qianqian, Ying Guangguo, Pan Changgui, et al. Comprehensive evaluation of antibiotics emission and fate in the river basins of China: source analysis, multimedia modeling, and linkage to bacterial resis-tance. Environmental science & technology, 2015, 49 (11): 72–82
[8] 国家环保局水和废水监测分析方法编委会. 水和废水监测分析方法. 第四版. 北京: 中国环境科学出版社, 2002
[9] 张衍, 陈吕军, 谢辉, 等. 两座污水处理系统中细胞态和游离态抗生素抗性基因的丰度特征. 环境科学, 2017, 38(9): 273–280
[10] Yoon Y, Chung H J, Wen Di D Y, et al. Inactivation efficiency of plasmid-encoded antibiotic resistance genes during water treatment with chlorine, UV, and UV/H2O2. Water Research, 2017, 123(7): 83–93
[11] 杨继平. 天津海河流域抗生素抗性基因分布特征及与指示微生物的关系[D]. 南昌: 南昌大学, 2017
[12] Lorenzo P, Adriana A, Jessica S, et al. Antibiotic resistance in urban and hospital wastewaters and their impact on a receiving freshwater ecosystem. Chemos-phere, 2018, 206: 70–82
[13] Mcconnell M M, Hansen L T, Neudorf K D, et al. Sources of antibiotic resistance genes in a rural river system. Journal of Environmental Quality, 2018, 47-(5): 997–1005
[14] Narciso-Da-Rocha C, Rocha J, Vaz-Moreira I, et al. Bacterial lineages putatively associated with the dis-semination of antibiotic resistance genes in a full-scale urban wastewater treatment plant. Environment International, 2018, 118(1): 79–88
[15] Xu Yanbin, Hou Maoyu, Li Yafei, et al. Distribu- tion of tetracycline resistance genes and AmpC β-lactamase genes in representative non-urban sewage plants and correlations with treatment processes and heavy metals. Chemosphere, 2017, 170(2): 74–81
[16] Börjesson S, Mattsson A, Lindgren P E, et al. Genes encoding tetracycline resistance in a full-scale muni-cipal wastewater treatment plant investigated during one year. Journal of Water and Health, 2010, 8(2): 247–256
[17] 张明美. 污水处理系统中抗生素抗性基因污染研究[D]. 杭州: 浙江大学, 2013
[18] Ma Liping, Li A D, Yin Xiaole, et al. The prevalence of integrons as the carrier of antibiotic resistance genes in natural and man-made environments. Environ-mental science & technology, 2017, 51(10): 5721–5728
[19] 苏志国, 张衍, 代天娇, 等. 环境中抗生素抗性基因与Ⅰ型整合子的研究进展. 微生物学通报, 2018, 45(10):153–169
[20] Nõlvak H, Truu M, Oopkaup K, et al. Reduction of antibiotic resistome and integron-integrase genes in laboratory-scale photobioreactors treating municipal wastewater. Water Research, 2018, 142(3): 63–72
[21] 奚慧. 上海城市典型水体中抗生素性基因时空分布特征及其影响子研究[D]. 上海: 华东师范大学, 2018
[22] 杜雪. 南昌市四种典型地表水体抗生素污染特征与生态风险评估[D]. 南昌: 南昌大学, 2015
[23] Yuan Qingbin, Guo Meiting, Yang jian. Monitoring and assessing the impact of wastewater treatment on release of both antibiotic-resistant bacteria and their typical genes in a Chinese municipal wastewater treatment plant. Environ Sci Process Impacts, 2014, 16(8): 1930–1937
Variations of 4 Antibiotic Resistance Genes in a Sewage Treatment Plant
BAO Yingyu1, XIE Hui2, CHEN Lüjun2, WEN Donghui1,†
1. College of Environmental Sciences and Engineering, Peking University, Beijing 100871; 2. School of Environment, Tsinghua University, Beijing 100084; † Corresponding author, E-mail: dhwen@pku.edu.cn
Abstract In order to understand the variations of antibiotic resistance genes (ARGs) in sewage treatment plants(STPs), the distribution and removal efficiencies of 4 subtypes of intracellular ARGs (sulII, ermB, tetC and blaPSE-1) and class I integron integrase gene (intI1) in amiddle-scale STP in Hebei Province were detected by PCR and real-time fluorescent quantitative PCR (qPCR). 4 ARGs and intI1 were found in all water samples and 1.26–2.30 orders of magnitude of ARGs were removed by the STP. Correlation analysis showed that intI1 and water quality factors including pH, COD, and NH3-N might affect the distribution and diffusion of tetC, ermB, and blaPSE-1. The final effluent of a STP may promote the spread of ARGs in surface water system.
Keywords antibiotic resistance genes (ARGs); sewage treatment plants (STPs); A2/O process; real-time fluorescence quantitative PCR (qPCR)
doi: 10.13209/j.0479-8023.2020.046
国家自然科学基金(51678003, 51678334)资助
收稿日期: 2019–06–13;
修回日期: 2019–10–31